政策法規 || 《阿爾茨海默病治療藥物臨床試驗技術指導原則(征求意見稿)》(附法規概覽09.23-09.30)
01
關于公開征求《存在未滿足臨床需求的嚴重細菌性疾病患者抗菌藥物臨床研發技術指導原則(征求意見稿)》意見的通知
耐藥菌感染是全球關注的重要公共衛生問題。細菌耐藥問題導致嚴重細菌感染性疾病患者發病率逐年增加且缺乏有效治療手段。對于治療選擇有限或缺乏的存在未滿足臨床需求的患者,迫切需要新的、有效且安全的抗菌藥物。該類患者病情重、早期病原學診斷困難、常需要多種抗菌藥物聯合使用等,使嚴重細菌性疾病患者抗菌藥物臨床試驗的設計、開展以及研究結果的評估面臨巨大挑戰。為滿足此類抗菌藥物創新研發的需要,藥品審評中心起草了《存在未滿足臨床需求的嚴重細菌性疾病患者抗菌藥物臨床研發技術指導原則》,現形成征求意見稿。
掃描圖中二維碼
查看詳細信息

02
關于公開征求《阿爾茨海默病治療藥物臨床試驗技術指導原則(征求意見稿)》意見的通知
阿爾茨海默病屬于重大公共衛生領域疾病,是創新藥物研發的熱點和難點。為給業界人員在臨床研發路徑和臨床試驗設計方面提供參考,提高臨床研發效率,藥品審評中心起草了《阿爾茨海默病治療藥物臨床試驗技術指導原則》,已形成征求意見稿。

掃描圖中二維碼
查看詳細信息

01
國家藥監局關于發布參棗健腦口服液非處方藥說明書范本的公告(2024年第118號)

掃描圖中二維碼
查看詳細信息

02
國家藥監局關于中藥保護品種的公告(延長保護期第17號) (2024年第116號)

掃描圖中二維碼
查看詳細信息

03
中藥保護品種公告(第19號) (2024年第117號)
掃描圖中二維碼
查看詳細信息

04
2024年09月26日中藥品種保護受理公示

掃描圖中二維碼
查看詳細信息

CDE
01
國家藥監局藥審中心關于發布《地屈孕酮片生物等效性研究技術指導原則》《復方甘草酸苷片生物等效性研究技術指導原則》2項技術指導原則的通告(2024年第40號)

掃描圖中二維碼
查看詳細信息

02
關于公開征求《地中海貧血基因治療產品臨床試驗技術指導原則(征求意見稿)》意見的通知

掃描圖中二維碼
查看詳細信息

03
國家藥監局藥審中心關于發布《疫苗免疫原性橋接臨床試驗技術指導原則(試行)》的通告(2024年第41號)

掃描圖中二維碼
查看詳細信息

04
關于公開征求《地拉羅司分散片生物等效性研究技術指導原則(征求意見稿)》等5個生物等效性指導原則意見的通知
掃描圖中二維碼
查看詳細信息

05
關于公開征求《生物類似藥說明書撰寫技術指導原則(征求意見稿)》意見的通知

掃描圖中二維碼
查看詳細信息

ADR
01
非處方藥轉換枸櫞酸鉍鉀顆粒的公示
掃描圖中二維碼
查看詳細信息

02
非處方藥轉換蒲地藍消炎口服液的公示
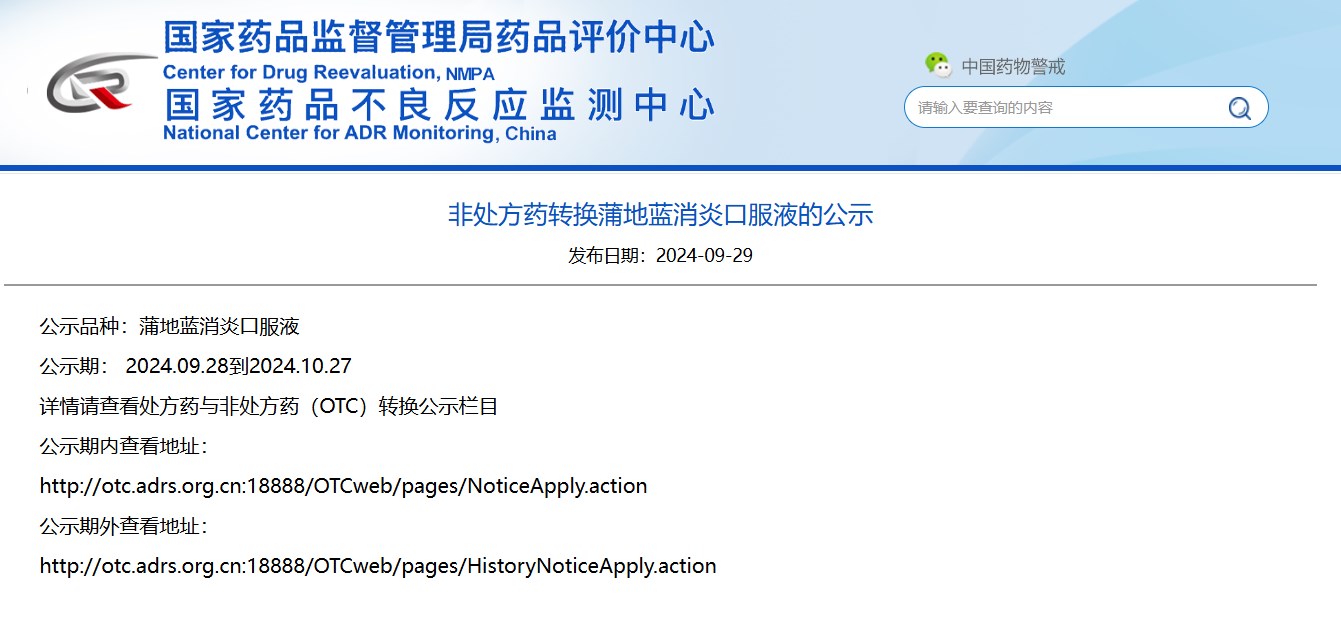
掃描圖中二維碼
查看詳細信息

藥典委
近期,藥典委發布的標準草案公示如下:
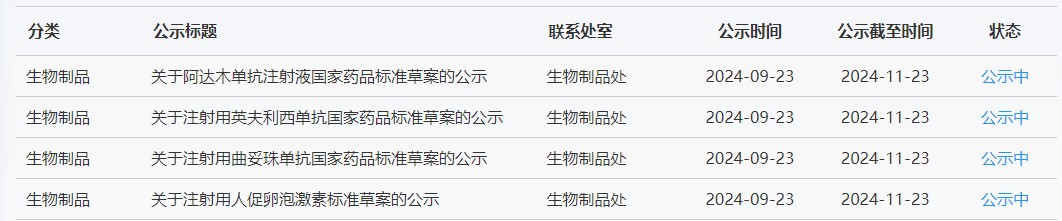
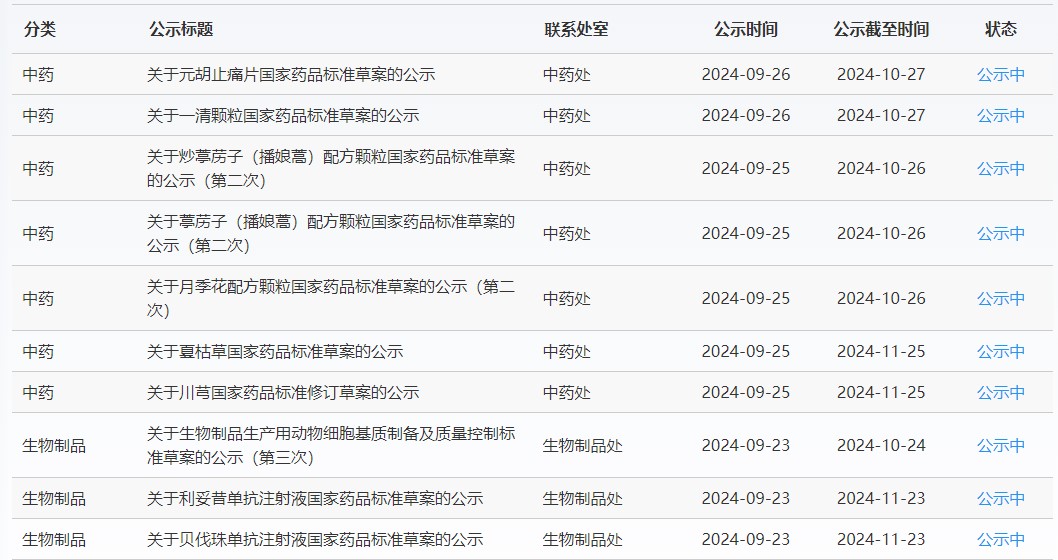
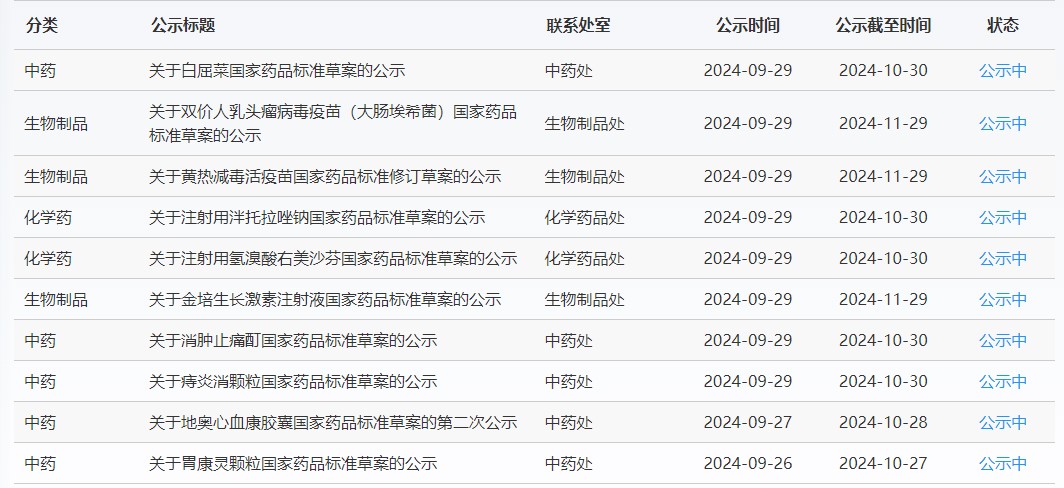
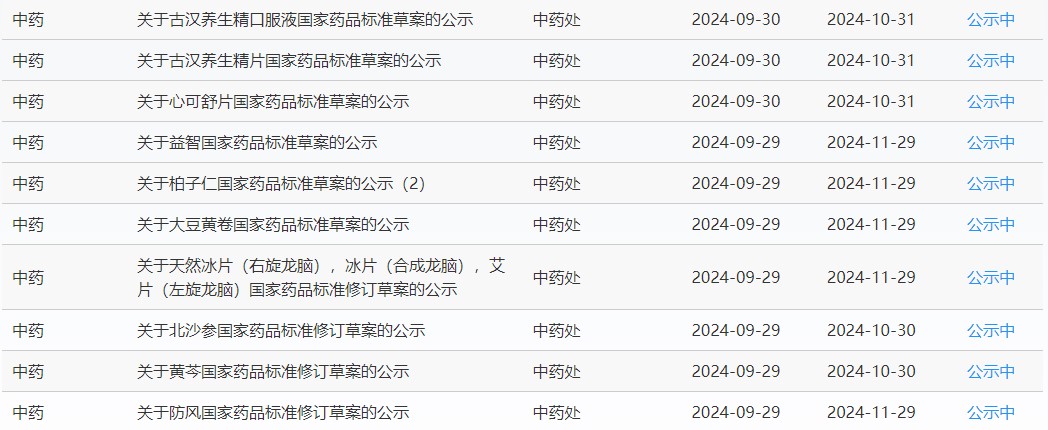
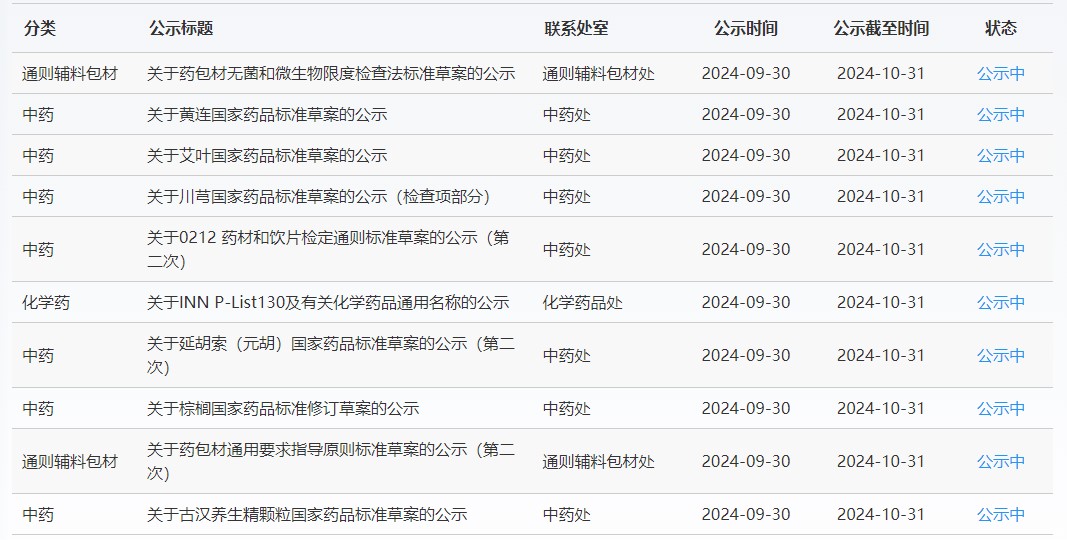
-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
