【干貨】人、機、料、法、環,全面解析,請查收!
“百年大計,質量第一”。黨的十八大以來,在以習近平同志為核心的黨中央堅強領導下,我國質量事業實現跨越式發展,質量強國建設取得歷史性成效。全民質量意識顯著提高,質量管理和品牌發展能力明顯增強。
醫藥行業作為關乎國家安全和人民健康的重要行業,具有更高的嚴謹性和責任意識。以臨床所需高質量藥品為目標,以各國藥品管理法、藥品注冊管理辦法、GMP以及相關的法律法規為依據,建立精細的研發管理體系、建立完善產品質量控制管理體系以及檢驗檢測體系,確保研究和開發的過程符合相關法規要求,確保每批藥品都符合相關藥典的規范,是醫藥企業的共同追求,也是研發企業穩步發展的護航之力。國際化、規范化、制度化的質量管理,不僅保障了高質量藥品的穩定輸出,保障人民用藥安全,還為贏得國際市場的認可奠定基礎,提高我國醫藥的國際競爭力。在“高質量”成果的加持下,“質量”將成為開啟世界醫藥市場的鑰匙,打入并屹立于世界醫藥之巔,指日可待!
下面我們通過新領先醫藥為例,詳細介紹醫藥行業“人機料法環”全方面的質量管控:
質量管理,以人為本。首先,我們必須明確的是,醫藥研發是一項高度專業且責任重大的工作,它關乎人類的生命與健康。因此,培養員工對于醫藥研發的敬畏心是至關重要的。這不僅要求員工具備扎實的專業知識和技能,更需要對生命和科學保持一顆敬畏之心。只有這樣,員工才能在研發過程中始終保持高度的責任心和敬業精神,確保每一項研發工作的嚴謹性和安全性。同時,敬畏心也能促使員工不斷自我反省和提升,以更加專業和負責的態度投入到醫藥研發工作中。因此,我們必須將敬畏心的培養作為醫藥研發團隊建設的重要一環,通過各種途徑和方法,引導員工樹立正確的價值觀和職業操守,以確保醫藥研發工作的順利進行,為人類的健康事業做出更大的貢獻。

其次,過硬的專業技能和對法規的充分理解尤為重要,新領先通過對人員進行入職培訓及考核,借助人員對比實驗以及中檢院能力認證,確保人員素質以及所用儀器技術掌握達到熟練程度、人員技術水平滿足研發需求、人員具備質量意識。此外,通過定期法規培訓提高人員質量管理理論能力、定期知識培訓鞏固人員熟知質量管理要求,提升自我保護的意識、風險意識,避免出現質量事故。
機(儀器)
“工欲善其事,必先利其器”,在醫藥研發過程中,各種儀器設備扮演著至關重要的角色,它們是獲取準確數據、驗證實驗結果的重要工具。因此,企業必須按規定期對儀器設備進行完整的質量控制。

從儀器購買開始,要進行嚴格的供應商篩選,按照URS進行招標采購。設備入場過程中,需要專業的工程師團隊進行3Q確認(IQ(安裝確認)、OQ(運行確認)和PQ(性能確認)),在儀器使用周期內,按照使用周期進行第三方計量,確保準確性,并注明校準有效期。
其次,對這些儀器進行日常的內部校驗和維護保養,是確保研發工作順利進行的關鍵措施,通過定期的校驗,可以及時發現儀器設備的誤差或異常,從而避免因設備問題導致的實驗結果偏差或誤判。而有效的維護保養則能延長儀器設備的使用壽命,降低故障率,提高工作效率。為了確保儀器日常校驗和維護保養工作的有效開展,需要建立完善的制度和操作規程,明確責任分工和執行流程。同時,加強對員工的培訓和教育,提高他們對儀器設備的重視程度和維護技能。此外,對于一些精密、貴重的儀器設備,由專業人員進行使用、檢修和保養,以確保其性能和精度始終保持在最佳狀態。總之,儀器日常的內部校驗和維護保養工作是醫藥研發工作中不可或缺的一環,它不僅關系到研發數據的準確性和可靠性,更直接影響到研發成果的質量和水平。因此,我們必須給予足夠的重視和投入,確保這一工作的有效開展。
對儀器的故障的基本判斷和簡單維修,也是實驗員應當具備的素質。積累和總結現象和經驗,能夠快速識別和處理實驗過程中90%的儀器設備問題。如不能自行處理,應報設備管理部門進行處理解決。
料(物料)
在物料管理方面,企業應采取一系列措施確保研發過程中的物料得到妥善管理。首先,建立專門的物料管理部門對涉及到的原料、雜質、試劑、輔料、對照品、包材等進行統一管理是必要的。對于有實力的企業,引入數智化的線上物料管理系統能更高效地管理物料存量、效期和領用記錄,便于及時補充和追溯使用情況。
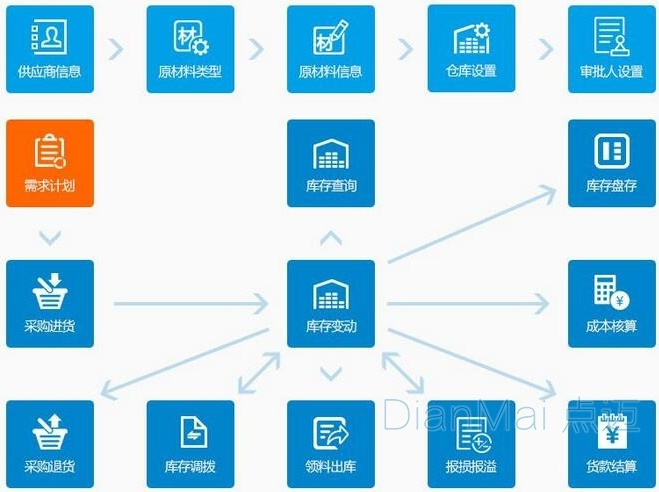
其次,質量控制應從源頭抓起。企業應審計物料來源,嚴格把關。對于外購的實驗用樣品,如原料藥、雜質等,應要求附有原廠COA,并在入庫前進行純度標化和性狀檢查,同時確認其結構并附上標化圖譜。領用人需按需領用并登記使用用途、用量和剩余量,遵循法規和相關制度要求,確保使用受控的出入庫臺賬和受控表格記錄等文件,規范物料流通管理。
此外,實驗員在取用物料時需注意確保物料在效期內,并關注批間差異。剩余物料應及時入庫,以防與其他物質接觸造成污染。在使用試劑時,應注意級別問題,特別是涉及危險試劑的使用安全問題(危化品庫管理辦法)。
法(方法)
在藥品研發過程中,方法、制度流程是至關重要的,它不僅關系到產品的安全性和有效性,更是企業持續發展的基石。
首先,我們必須深入學習和嚴格遵守國家層面的法律法規、藥典標準以及國際公認的ICH指導原則。這些是國家對藥品研發的基本要求,也是行業共識的體現。企業應定期組織相關培訓,確保每個員工都清楚自己的職責和操作要求。

其次,企業也必須制定并執行一套完善的流程體系,這不僅能夠規范實驗員的日常操作,確保實驗結果的準確性和可靠性,還能有效減少誤差。而且,隨著法規的更新和技術的進步,企業應不斷優化SOP內容,確保其始終與最新法規和行業標準保持一致。
為了確保藥品研發過程的合規性,企業還應配合相關工作機制、流程以及質量管理制度。這不僅包括研發過程中的質量控制,也包括注冊審批階段的文件準備和審核。通過這樣的綜合管理,企業可以確保研發過程符合國家法規要求,進而確保注冊審批的順利通過。
環(環境)
環境因素往往是最容易被忽視的環節。然而,隨著企業走向國際化和GMP理念的深入貫徹,環境管理已經成為首要任務。實驗室的布局設計、環境控制以及危險品的依法標識和廢液處理都至關重要。

值得注意的是,許多OOS、OOT和異常情況都與環境因素有關。因此,對環境因素的關注和管理是減少實驗誤差和確保數據可靠性的關鍵。特別是對于一些敏感性藥品,其對溫濕度和光照的要求異常嚴格。因此,在日常操作過程中,實驗員應關注環境條件的調節,如避光操作和除濕操作等。穩定性放樣室對于環境的要求更高,應具備恒溫、恒濕和防塵等環境控制功能,以滿足藥品穩定性試驗的要求,定期監測并記錄室內溫濕度等環境參數,確保其符合預設標準。
為了實現有效的環境管理,企業應采取一系列措施。首先,實驗室的布局設計應符合GMP理念,確保實驗操作流程合理、安全且符合法規要求。其次,實驗室應配備先進的環境控制系統,如溫濕度調節設備、空氣凈化系統等,以確保實驗環境始終處于最佳狀態。此外,危險品的標識和廢液處理也應依法進行,以保障實驗員的安全和環境的可持續性。
如今在醫藥研發行業,“藥品全生命周期的質量管理”已成為醫藥企業共識。但相比于藥品生產環節質量管理的重視,許多企業往往會忽視藥品研發階段的質量管理。或許是受GMP的啟發和影響,偏差、變更、風險評估……這些關鍵詞正在被頻繁地運用在研發質量管理中,“研發QA”正在被賦予更多的職責和重任,藥品研發也越來越重視質量管理體系的建設。
新領先基于ISO9001國際標準,結合FDA、EMA、NMPA等監管細則,建立了具有新領先特色的質量管理體系,實現國際化、正規化、高效化的全面管理,能夠為客戶提供專業、優質、質量可靠的研發服務。
-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
