政策法規《化學仿制藥參比制劑目錄(第八十批)》(征求意見稿)(附法規概覽03.18-03.22)
01
關于公開征求《化學仿制藥參比制劑目錄(第八十批)》(征求意見稿)意見的通知
參比制劑是指用于仿制藥質量和療效一致性評價的對照藥品,通常為被仿制的對象,如原研藥品或國際公認的同種藥物,參比制劑應為處方工藝合理、質量穩定、療效確切的藥品。經國家藥品監督管理局仿制藥質量和療效一致性評價專家委員會審核確定,現發布仿制藥參比制劑目錄(第八十批)(征求意見稿),新增44個品規的參比名單;另外12個增加變更后上市許可持有人、增加上市許可持有人、不限定上市國及產地等。

掃描識別圖中二維碼
查看詳細信息

02
關于公開征求ICH《Q3C(R9):雜質:殘留溶劑的指導原則》實施建議和中文版意見的通知
為推動ICH指導原則在國內的平穩落地實施,國家藥品監督管理局藥品審評中心擬定了《Q3C(R9)指導原則實施建議》,同時組織翻譯了Q3C(R9)指導原則的中文版。現對該實施建議和中文版公開征求意見。

掃描識別圖中二維碼
查看詳細信息

01
2024年3月18日中藥品種保護受理公示

掃描識別圖中二維碼
查看詳細信息

02
國家藥監局關于阿膠當歸膠囊和芪參補氣膠囊轉換為非處方藥的公告(2024年第27號)

掃描識別圖中二維碼
查看詳細信息

03
國家藥監局關于修訂復方金銀花顆粒和普樂安制劑說明書的公告(2024年第28號)
掃描識別圖中二維碼
查看詳細信息

04
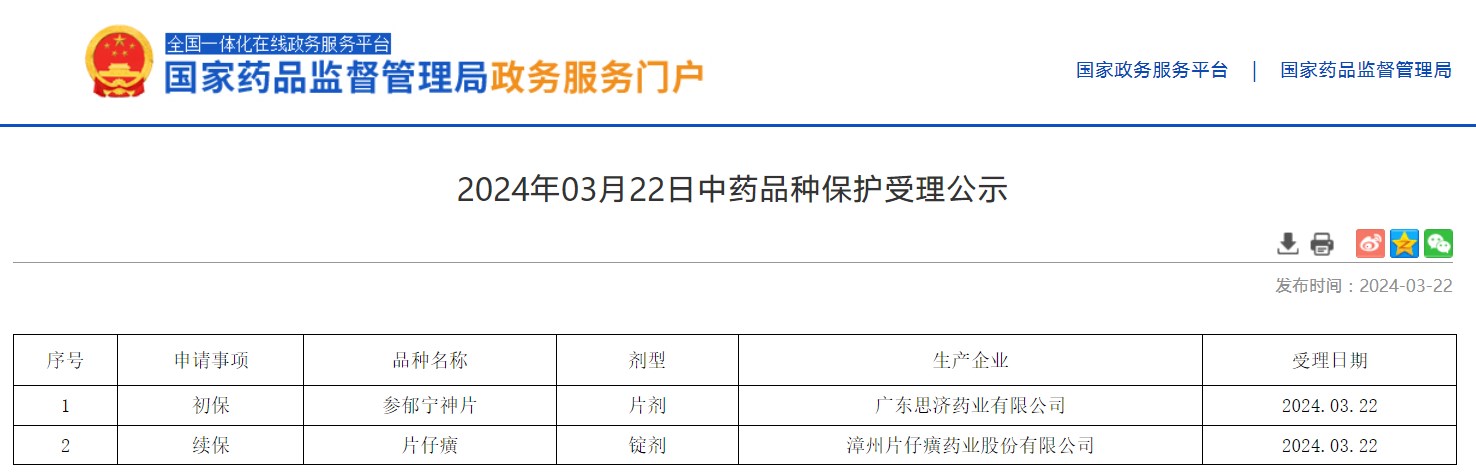
2024年03月22日中藥品種保護受理公示
掃描識別圖中二維碼
查看詳細信息

01
關于做好2024年度國家藥品標準提高工作的通知
掃描識別圖中二維碼
查看詳細信息

02
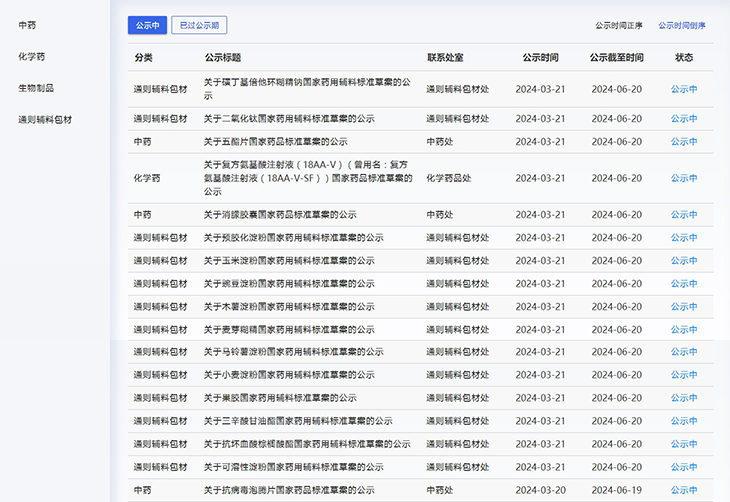
本周,藥典委發布的藥品及藥用輔料標準草案如下
掃描識別圖中二維碼
查看詳細信息

-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
