科普 | 我國藥品信息化追溯體系制度建設
發布時間:2023-04-26
藥品信息化追溯體系指的是藥品上市許可持有人、生產企業、經營企業、使用單位、監管部門、消費者等藥品追溯參與方,通過信息化手段,對藥品生產、流通、使用等各環節的信息進行追蹤、溯源的有機整體。本文結合政策法規,對藥品信息化追溯體系制度、相關發展歷程等內容進行分享。
藥品信息化追溯體系分為藥品追溯系統、藥品追溯協同服務平臺、藥品追溯監管系統三個部分。
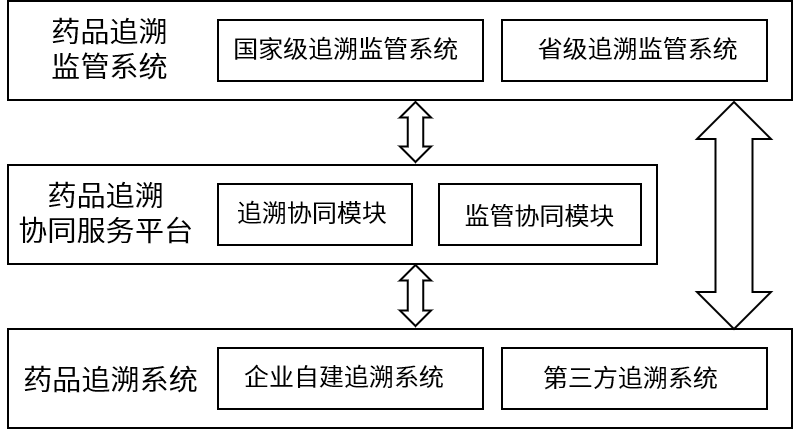
▲ 藥品信息化追溯體系構成框架
以藥品追溯系統為基礎,由藥品上市許可持有人自建或第三方服務商幫助企業建立,并向藥品流通、經營企業、藥品使用單位提供使用;藥品追溯協同服務平臺相當于連接樞紐中心,與國家監管追溯平臺對接,實現動態追溯。如果涉及進出口業務,需與國際平臺對接。
02 藥品信息化追溯體系建立發展脈絡
我國藥品追溯體系的建立歷經近20年的時間,從對疫苗、麻醉藥品、精神藥品、血液制品等特殊藥品和國家集中采購藥品實現“一物一碼,物碼同追”;到基本藥物、醫保報銷藥物等消費者普遍關注的產品,正逐步完善藥品信息化追溯體系。
2006: 我國對麻醉藥品和第一類精神藥品實行電子監管。
2008: 對第二類精神藥品和部分高風險藥品生產出廠、流通的動態監控,確保藥品真實、可追溯。2008.11.01起,對“四大類”高風險產品(血液制品、疫苗、中藥注射劑和二類精神藥品)實施電子監管。
2010: 電子監管范圍擴大到307種基本藥物。要求2011.04.01起,列入基本藥物目錄的品種,未入網及未使用藥品電子監管碼統一標識的,一律不得參與基本藥物招標采購。
2015: 2015年12月31日前,境內藥品制劑生產企業、進口藥品制藥廠商以及所有藥品批發、零售企業須全部入網。2016年1月1日后生產的藥品制劑應做到全部賦碼。
2016: 以推進藥品全品種、全過程追溯與監管為主要內容,建設完善藥品追溯體系;繼續推進藥品追溯系統的建立和完善,鼓勵藥品生產經營者運用信息技術建立藥品追溯體系;鼓勵行業協會組織企業搭建藥品追溯信息查詢平臺,為藥品生產經營者提供數據共享,為公眾提供信息查詢。
2018: 明確要求藥品上市許可持有人、生產企業、經營企業、使用單位通過信息化手段建立藥品追溯系統,及時準確記錄、保存藥品追溯數據,形成互聯互通藥品追溯數據鏈。
2019: 新《藥品管理法》正式生效,第十二條明確指出國家建立健全藥品追溯制度。
2020: 于2020年12月31日前,基本實現國家藥品集中采購中選品種、麻醉藥品、精神藥品、血液制品等重點品種可追溯。
2022: 藥品上市許可持有人應當建立并實施藥品追溯制度,按照規定賦予藥品追溯標識,建立信息化追溯系統;“十四五”期末需構建完善的藥品智慧監管技術框架,健全藥品信息化追溯體系,實現藥品重點品種可追溯。
03 藥品信息化追溯體系—藥品追溯碼
藥品追溯碼作為藥品信息化追溯體系的直接體現,如同藥品的電子身份證號碼。要求一物一碼,物碼同追,能夠確保藥品生產、流通和使用全過程來源可查、去向可追;有效防范非法藥品進入合法渠道;確保發生質量安全風險的藥品可召回、責任可追究。具有實用性、唯一性、可擴展性、通用性的特點。
藥品追溯碼用于唯一標識藥品各級銷售包裝單元的代碼,由一列數字、字母和(或)符號組成,包含藥品標識碼和生產標識碼。
? 藥品標識碼:用于標識特定于某種與藥品上市許可持有人、 生產企業、藥品通用名、劑型、制劑規格和包裝規格對應的藥品的唯一性代碼。
? 生產標識碼:用于識別藥品在生產過程中相關數據的代碼。
參考文件
《藥品信息化追溯體系建設導則》
《藥品追溯碼編碼要求》
《疫苗追溯數據交換基本技術要求》
《疫苗追溯基本數據集》
《藥品上市許可持有人和生產企業追溯基本數據集》
《藥品經營企業追溯基本數據集》
《藥品使用單位追溯基本數據集》
《藥品追溯消費者查詢基本數據集》
《藥品追溯數據交換基本技術要求》
《藥品追溯碼標識規范》
《藥品追溯消費者查詢結果顯示規范》
-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。




 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
