政策法規(guī)||?仿制藥參比制劑目錄(第五十九批)發(fā)布(附本周法規(guī)概覽09.26-09.30)
本周熱點(diǎn)
01
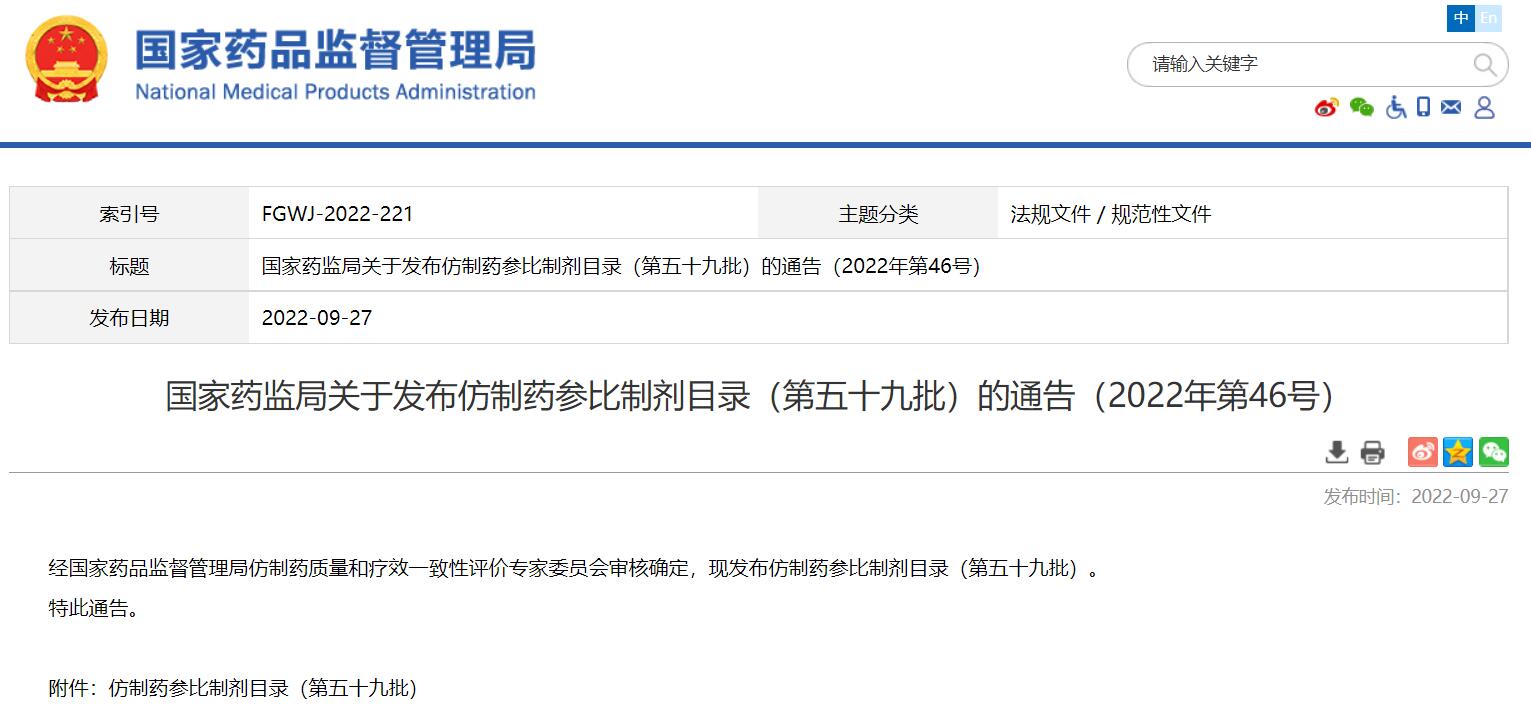
國家藥監(jiān)局關(guān)于發(fā)布仿制藥參比制劑目錄(第五十九批)的通告(2022年第46號(hào))
參比制劑是指用于仿制藥質(zhì)量和療效一致性評價(jià)的對照藥品,通常為被仿制的對象,如原研藥品或國際公認(rèn)的同種藥物,參比制劑應(yīng)為處方工藝合理、質(zhì)量穩(wěn)定、療效確切的藥品。
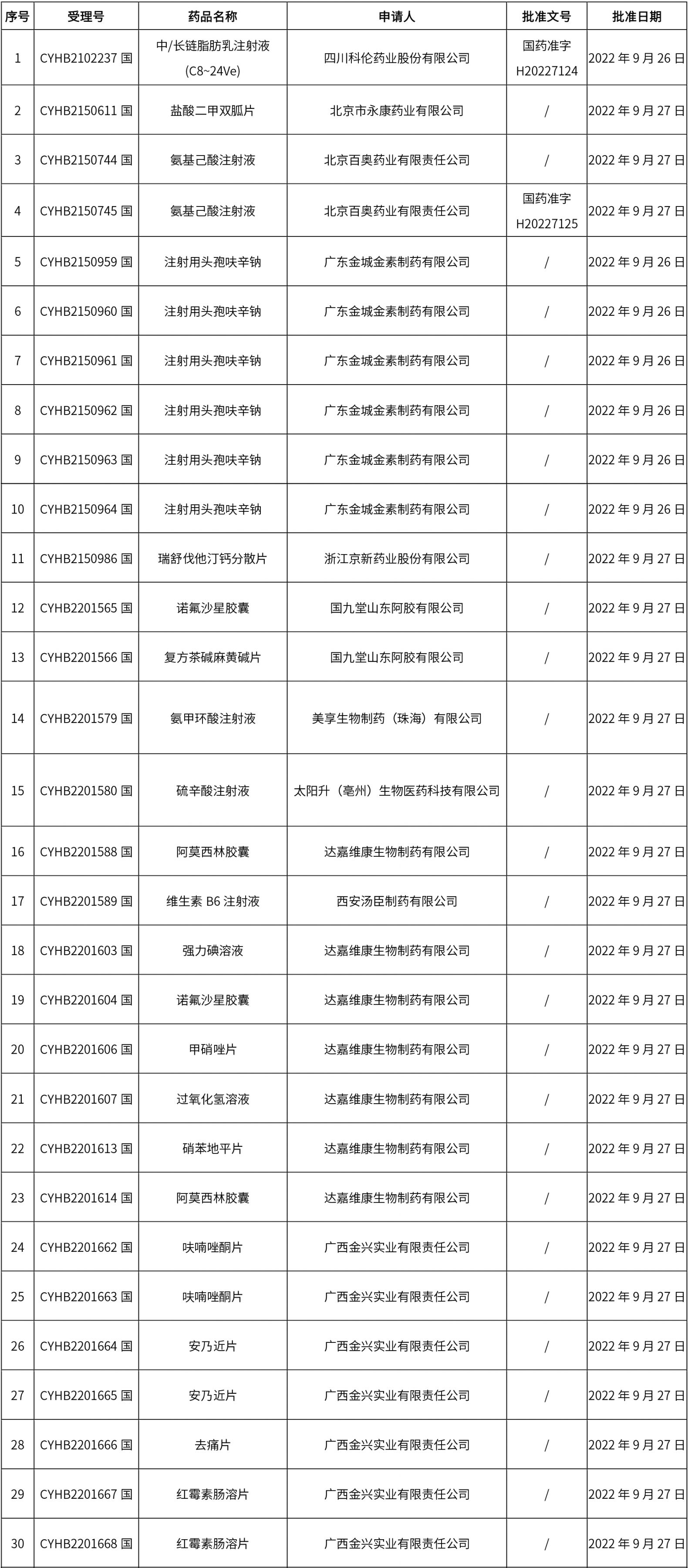
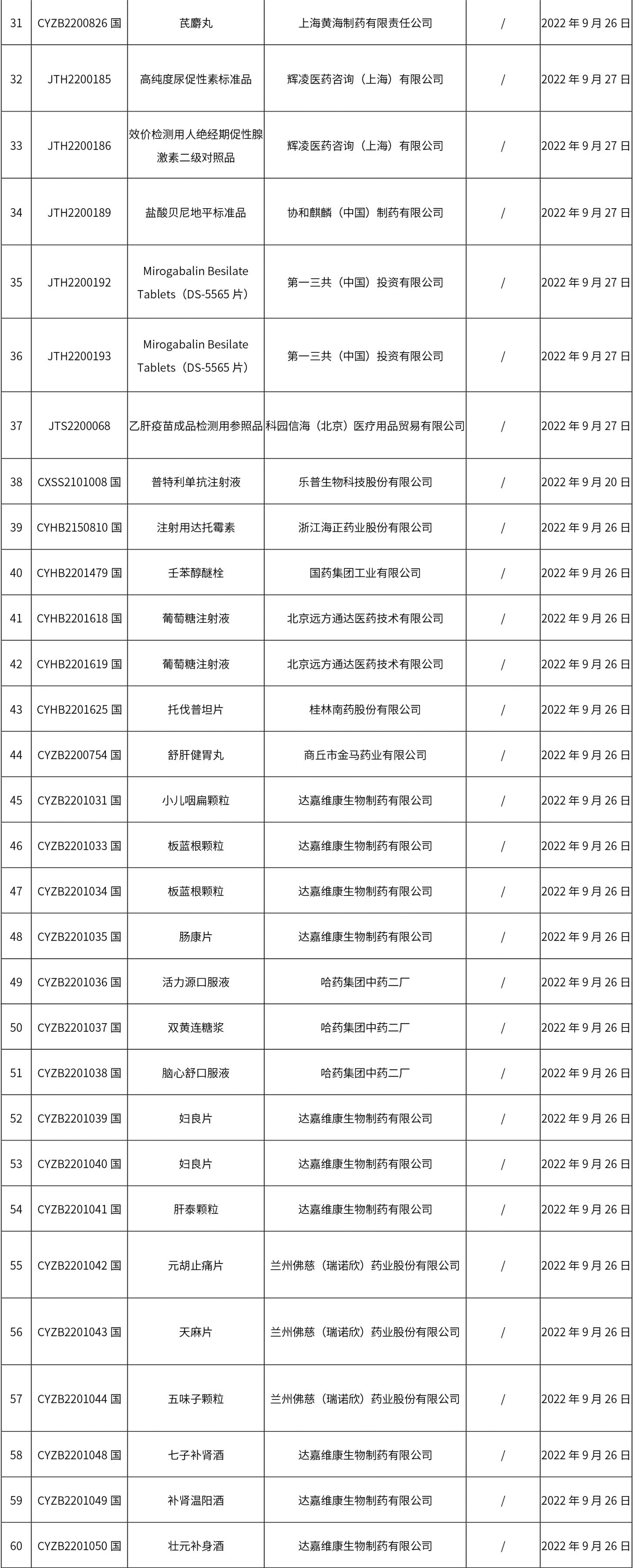
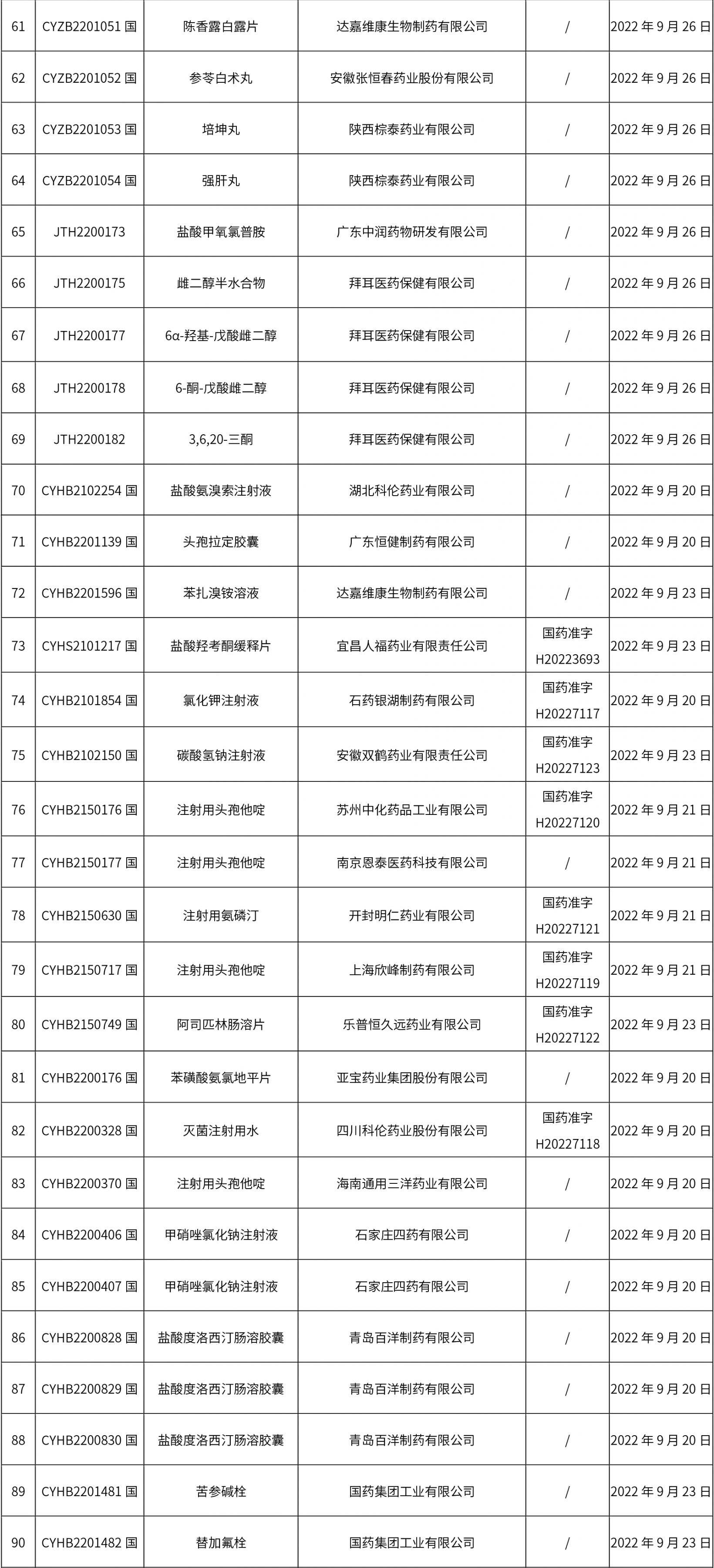
經(jīng)國家藥品監(jiān)督管理局仿制藥質(zhì)量和療效一致性評價(jià)專家委員會(huì)審核確定,現(xiàn)發(fā)布仿制藥參比制劑目錄(第五十九批),新增67個(gè)品規(guī)的參比名單;已發(fā)布化學(xué)仿制藥參比制劑增補(bǔ)目錄13個(gè),多為增加持證商,個(gè)別品規(guī)(噻托溴銨粉吸入劑/噻托溴銨吸入粉霧劑)是“修訂規(guī)格及藥品通用名稱”。
掃描識(shí)別圖中二維碼
查看詳細(xì)信息

02
國家藥監(jiān)局藥審中心關(guān)于發(fā)布《藥物臨床依賴性研究技術(shù)指導(dǎo)原則(試行)》的通告(2022年第35號(hào))
藥物臨床依賴性研究是具有潛在濫用風(fēng)險(xiǎn)的新藥上市前的重要研究內(nèi)容,我國尚無專門技術(shù)要求對此類研究進(jìn)行規(guī)范管理。
在國家藥品監(jiān)督管理局的部署下,藥審中心組織制定了《藥物臨床依賴性研究技術(shù)指導(dǎo)原則(試行)》根據(jù)《國家藥監(jiān)局綜合司關(guān)于印發(fā)藥品技術(shù)指導(dǎo)原則發(fā)布程序的通知》(藥監(jiān)綜藥管〔2020〕9號(hào))要求,經(jīng)國家藥品監(jiān)督管理局審查同意,于2022年9月26日發(fā)布,自發(fā)布之日起施行。

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

03
關(guān)于公開征求《咀嚼片(化學(xué)藥品)質(zhì)量屬性研究技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知
為明確對咀嚼片(化學(xué)藥品)質(zhì)量屬性研究的技術(shù)要求,以更好地指導(dǎo)企業(yè)進(jìn)行研究以及統(tǒng)一監(jiān)管要求,國家藥品監(jiān)督管理局藥品審評中心經(jīng)調(diào)研以及與專家和業(yè)界討論,組織起草了《咀嚼片(化學(xué)藥品)質(zhì)量屬性研究技術(shù)指導(dǎo)原則(征求意見稿)》。

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

04
關(guān)于公開征求《治療卵巢癌新藥臨床研發(fā)技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知
現(xiàn)階段國內(nèi)尚無治療卵巢癌新藥臨床研發(fā)相關(guān)技術(shù)指導(dǎo)原則,現(xiàn)有的指導(dǎo)原則尚不能涵蓋和專門針對卵巢癌的臨床試驗(yàn)設(shè)計(jì)的考慮,為進(jìn)一步明確技術(shù)原則,提高新藥研發(fā)效率,化藥臨床一部相關(guān)適應(yīng)癥小組組織撰寫了《治療卵巢癌新藥臨床研發(fā)技術(shù)指導(dǎo)原則》,形成征求意見稿,供藥物研發(fā)相關(guān)人員參考。

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

01
關(guān)于藥審中心與中國藥品監(jiān)督管理研究會(huì)合作舉辦“細(xì)胞和基因治療產(chǎn)品藥學(xué)研究與評價(jià)審評考慮”線上培訓(xùn)的通知

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

02
關(guān)于公開征求《基于人用經(jīng)驗(yàn)的中藥復(fù)方制劑新藥藥學(xué)研究技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

03
關(guān)于公開征求《中藥新藥臨床試驗(yàn)用藥品的制備研究技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知

掃描識(shí)別圖中二維碼
查看詳細(xì)信息

1. 本周(截止09.30中午12:15)共發(fā)布了211個(gè)品規(guī)的藥品批準(zhǔn)證明文件待領(lǐng)取信息,其中一致性評價(jià)27個(gè),注射劑51個(gè)(其中1個(gè)為滅菌注射用水)。
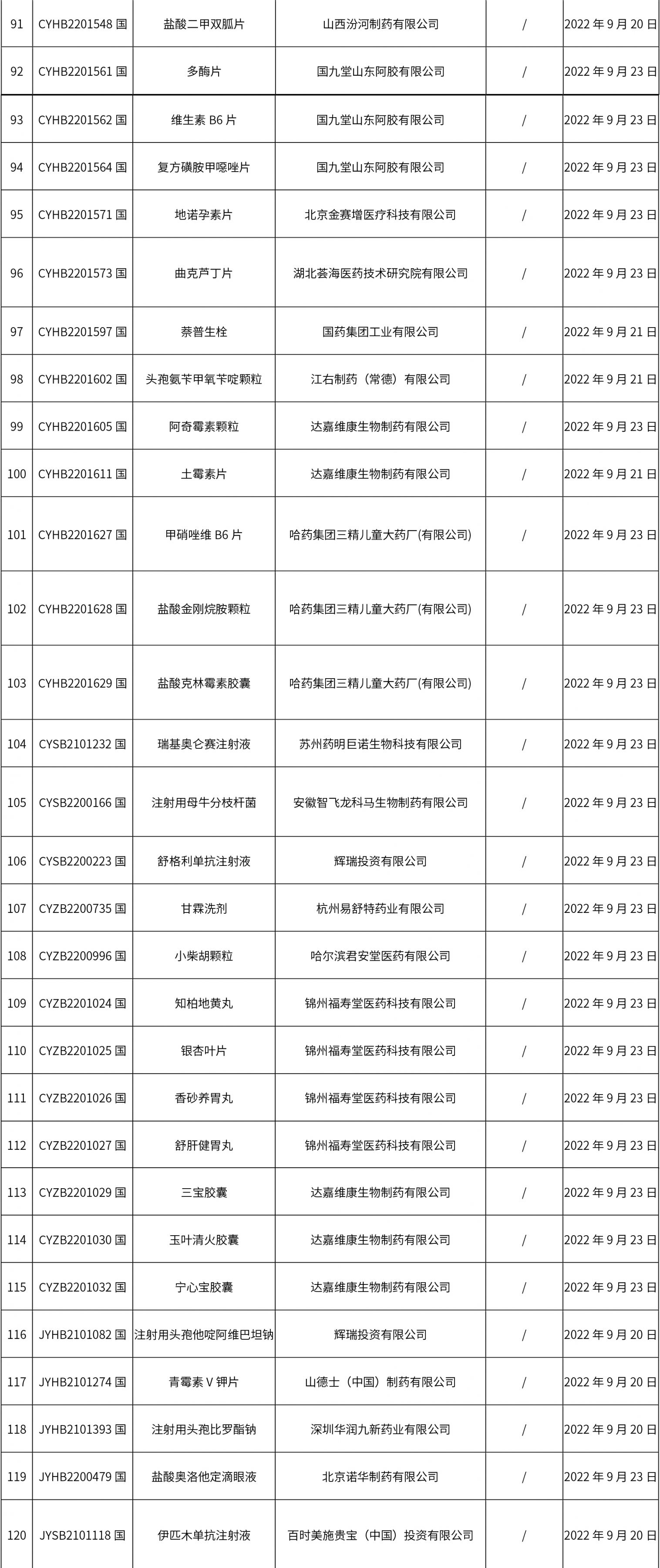
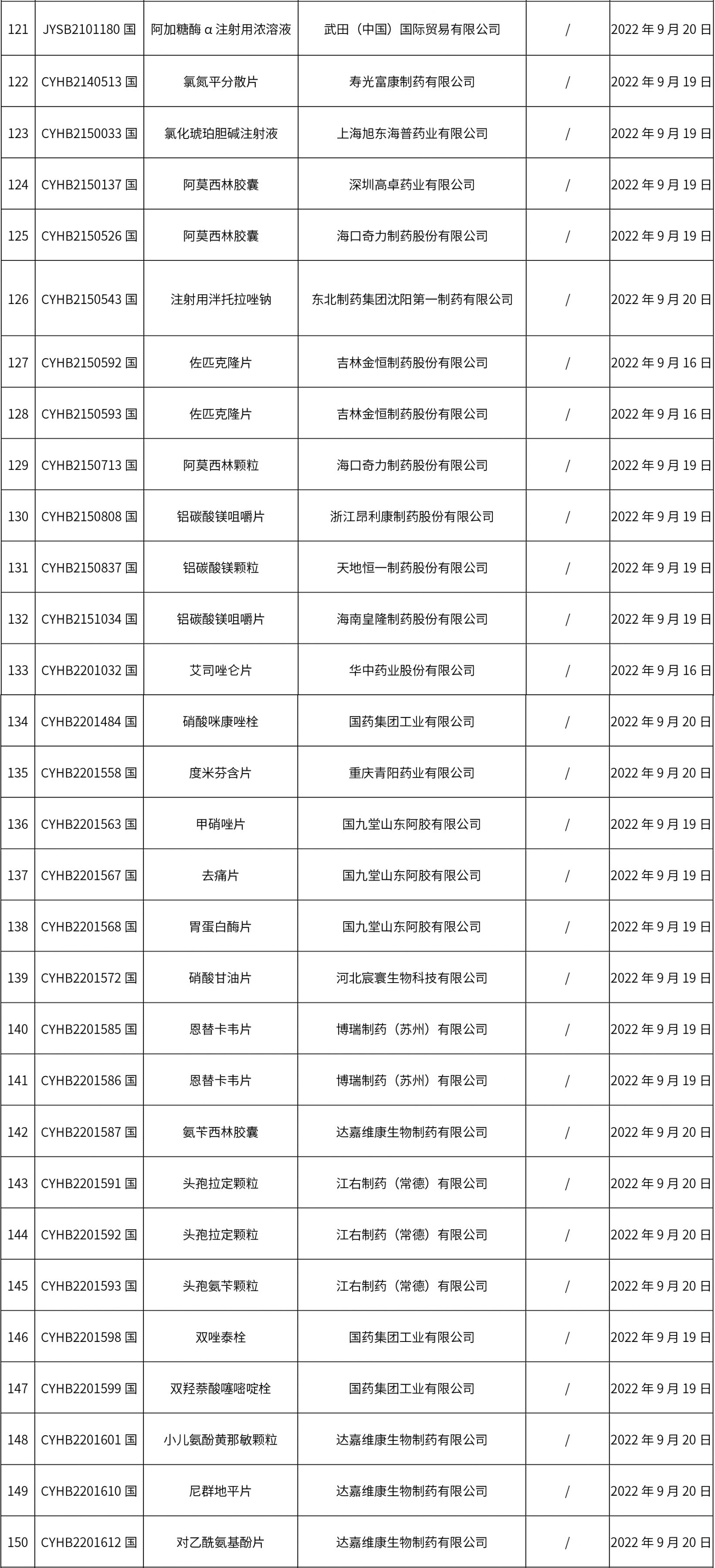
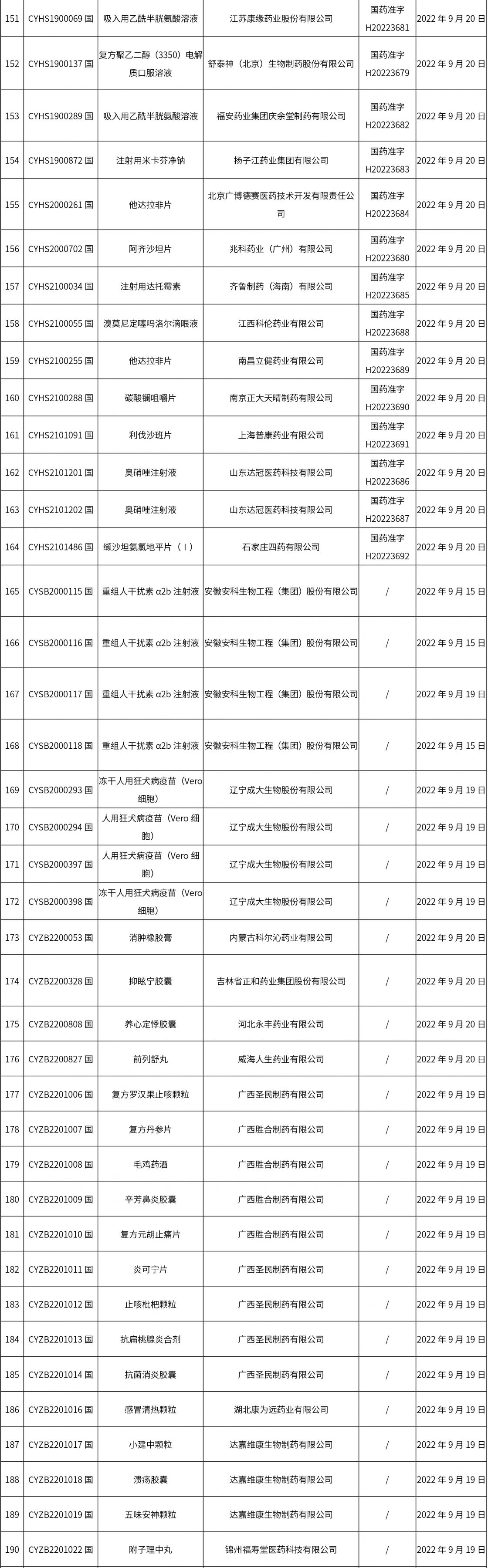
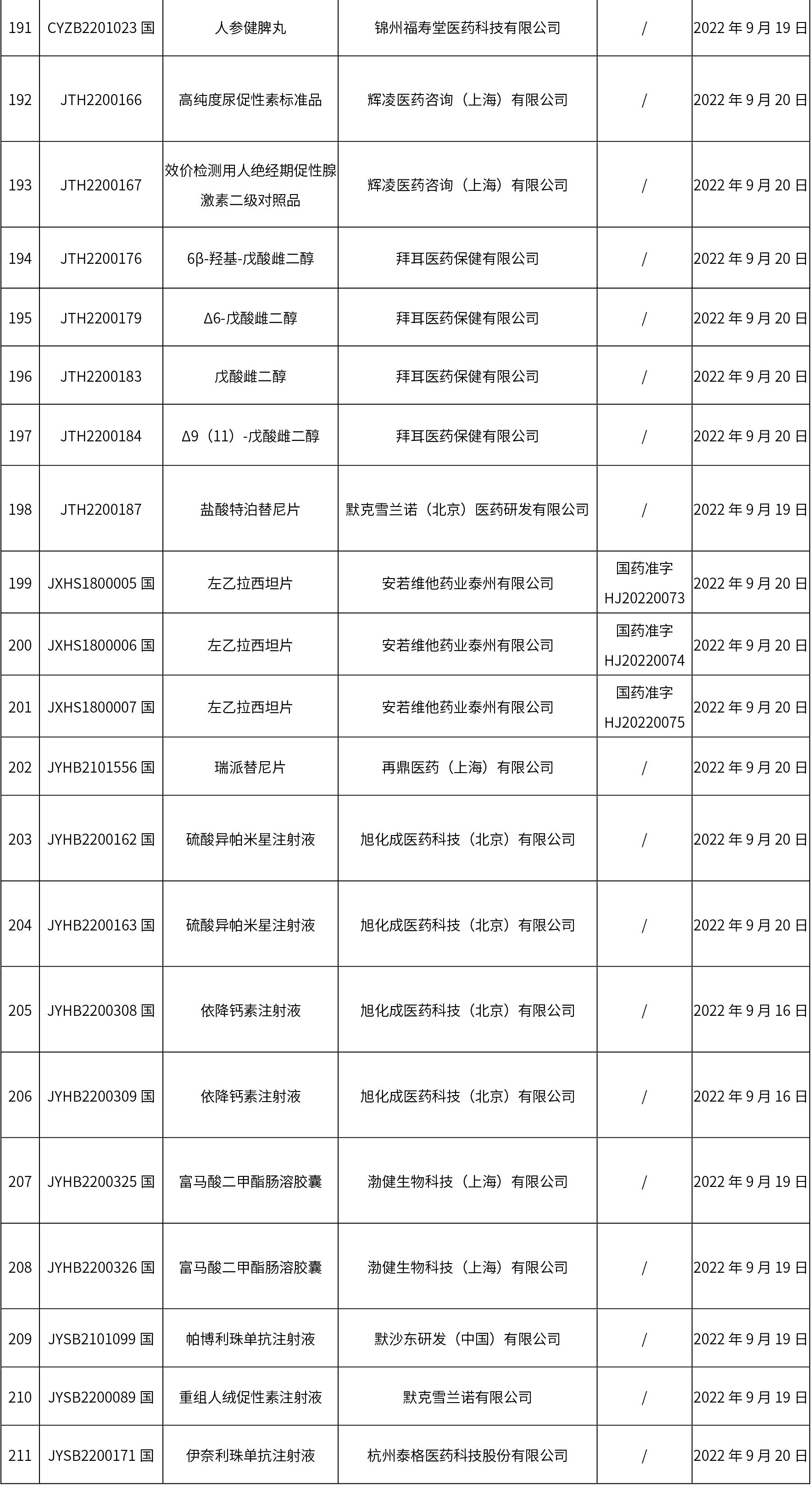
02
我國國產(chǎn)首臺(tái)質(zhì)子治療系統(tǒng)獲批上市
掃描識(shí)別圖中二維碼
查看詳細(xì)信息

03
國家藥監(jiān)局關(guān)于成立第十二屆藥典委員會(huì)的公告(2022年第80號(hào))
掃描識(shí)別圖中二維碼
查看詳細(xì)信息

04
.國家藥監(jiān)局關(guān)于緩繳藥品、醫(yī)療器械產(chǎn)品注冊費(fèi)的公告(2022年第81號(hào))
掃描識(shí)別圖中二維碼
查看詳細(xì)信息

1. 本周藥典委發(fā)布6個(gè)品種國家藥品/藥用輔料標(biāo)準(zhǔn)草案公示。
掃描識(shí)別圖中二維碼
查看詳細(xì)信息

-END-



轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務(wù)熱線:010-61006450
Hotline服務(wù)熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
