政策法規||?《成人用藥數據外推至兒科人群的定量方法學指導原則(征求意見稿)》發布(附本周法規概覽09.19-09.23)
發布時間:2022-09-23
01
關于《成人用藥數據外推至兒科人群的定量方法學指導原則(征求意見稿)》公開征求意見的通知
本指導原則主要闡述基于現有中國成人等數據外推至中國兒科人群的外推策略、主要定量方法及應用場景,從而為以注冊為目的基于成人用藥數據外推至兒科人群的藥物研發提供指導,也可供不同年齡段兒科人群數據外推以及以非注冊為目的的兒科人群的藥物研發參考。

掃描識別圖中二維碼
查看詳細信息

02
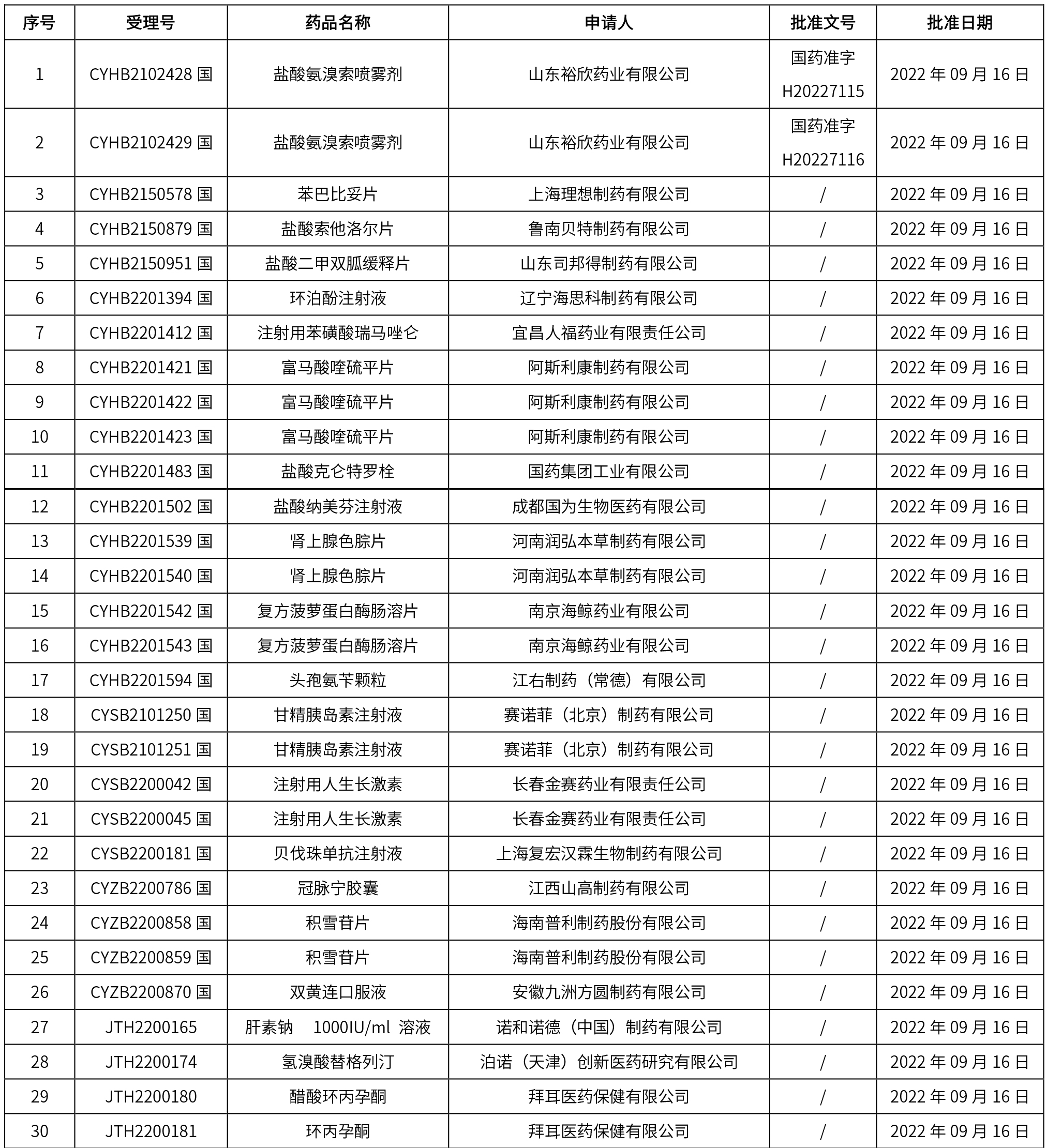
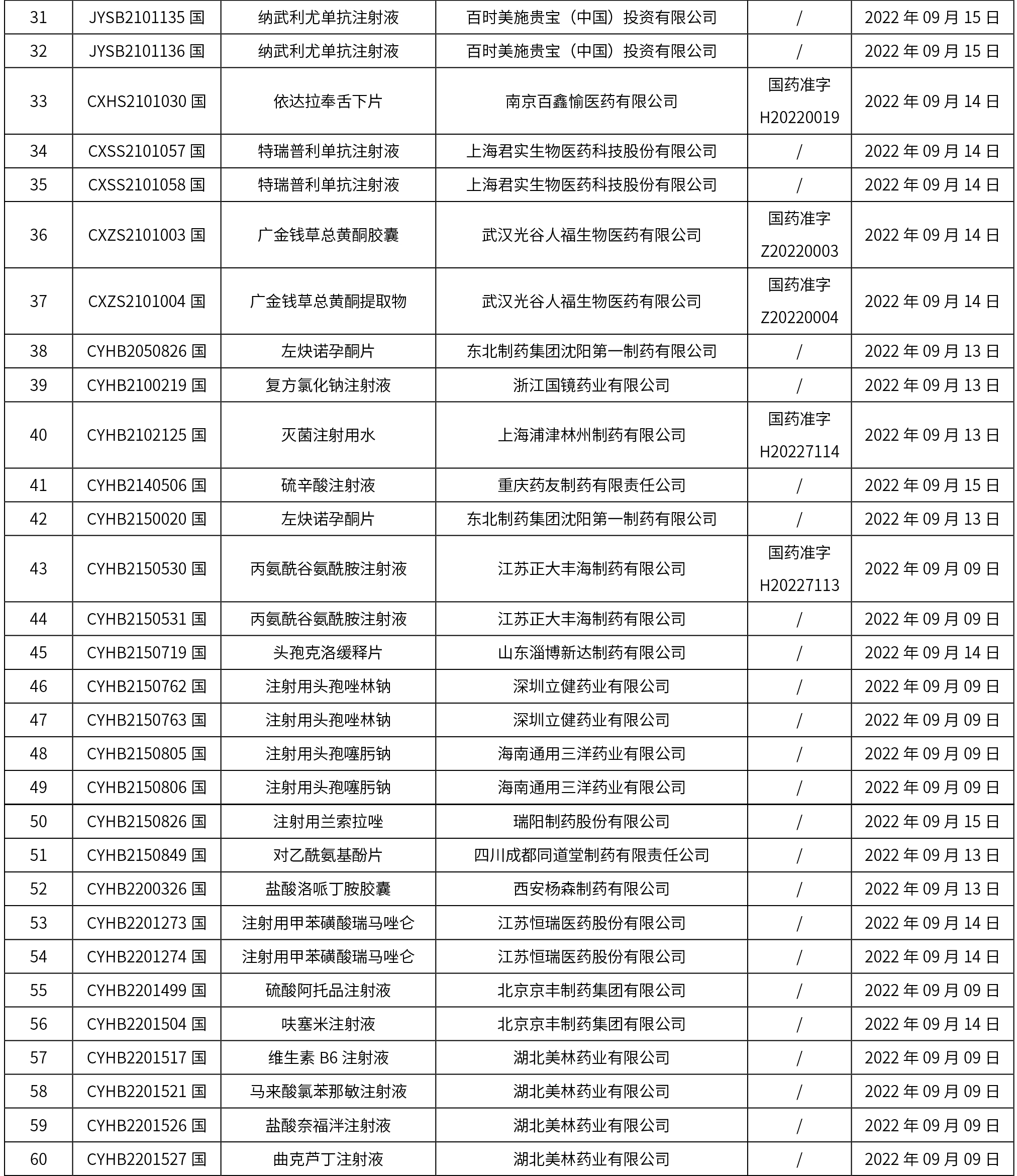
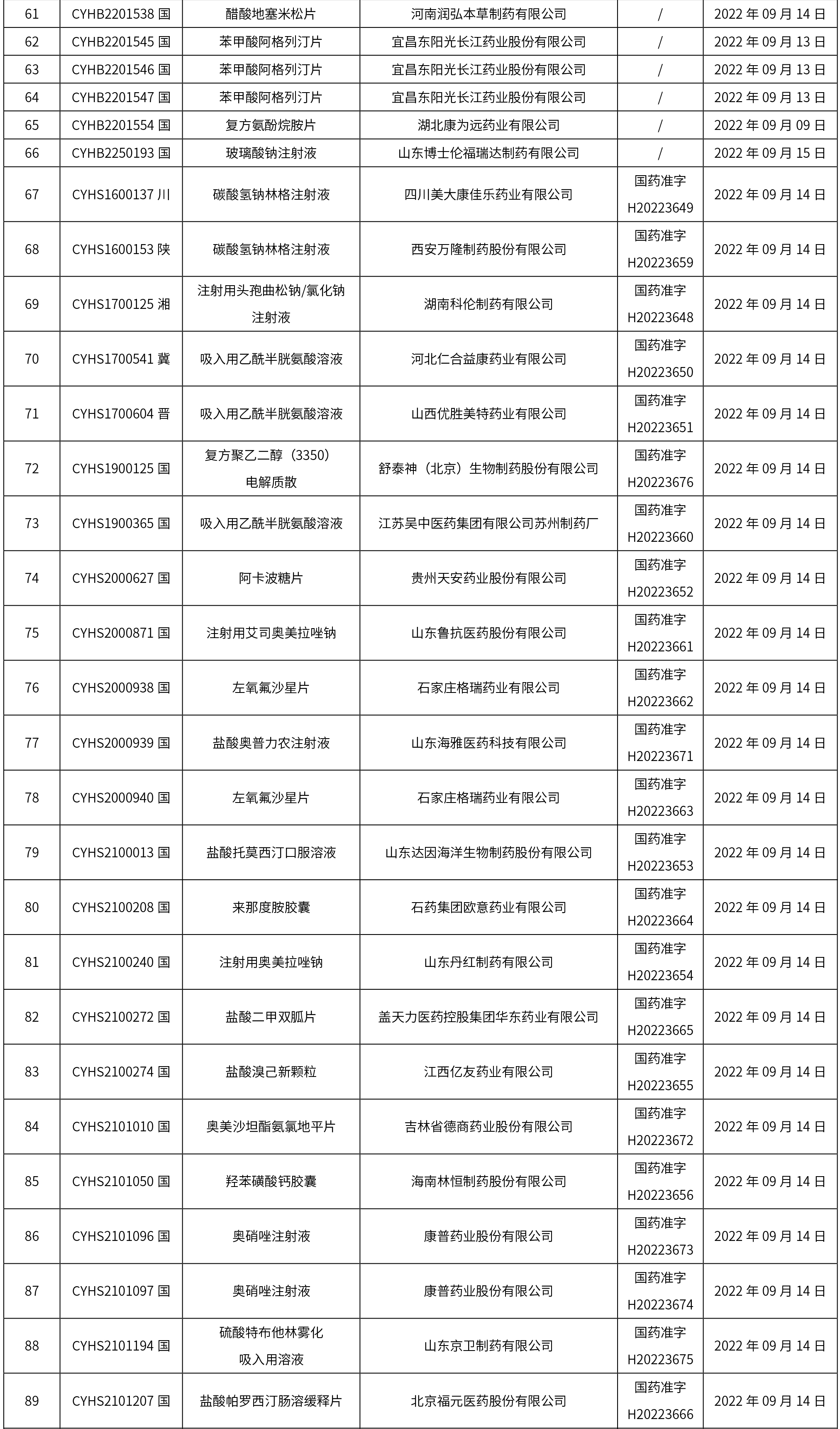
國家藥監局關于批準注冊210個醫療器械產品公告 (2022年8月) (2022年第78號)
掃描識別圖中二維碼
查看詳細信息

NMPA
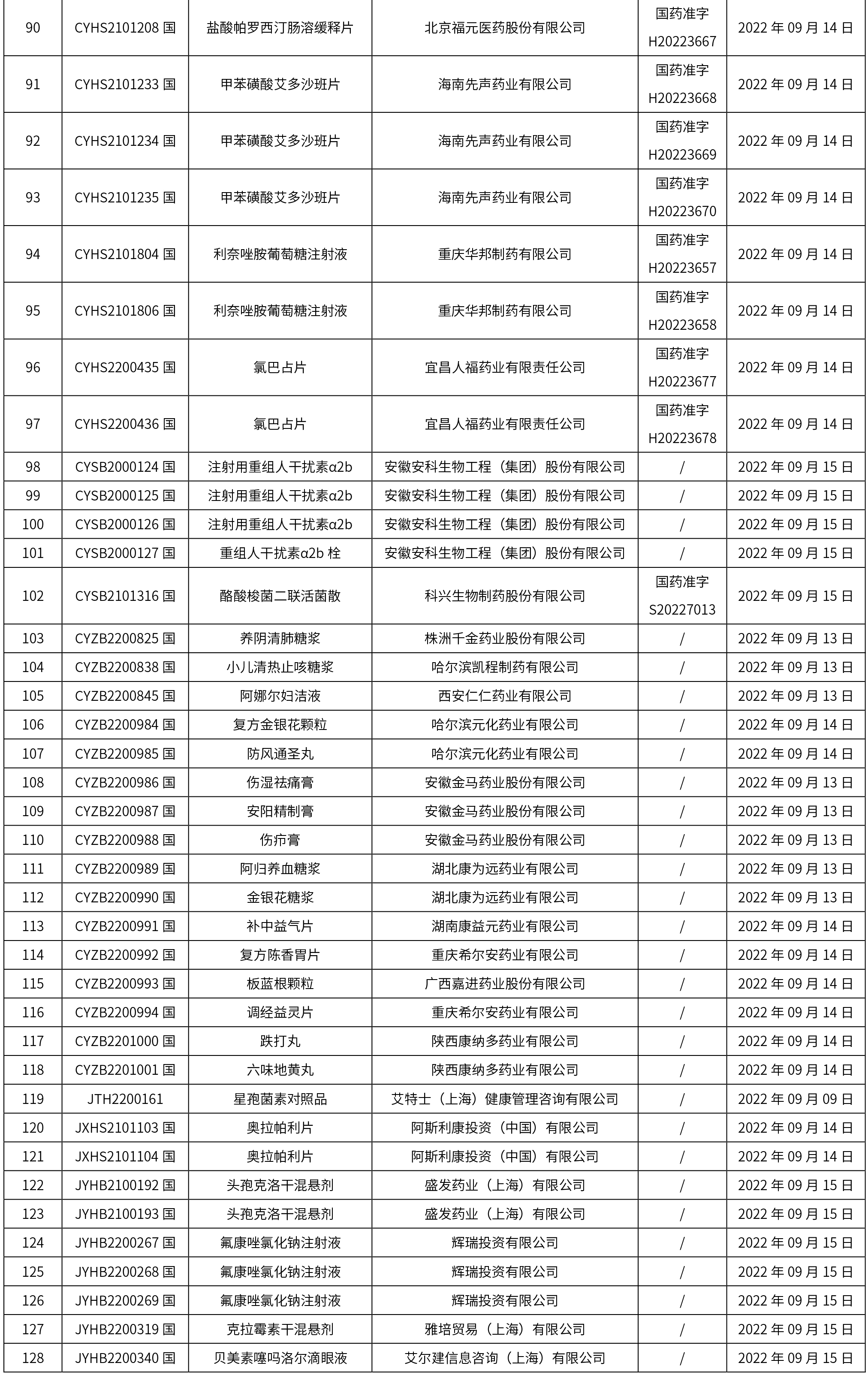
1. 本周(截止到9月23日12:00)共發布了128個品規的藥品批準證明文件待領取信息,其中一致性評價15個,注射劑30個。
02
京津冀聯合開展藥物臨床試驗質量管理檢查員培訓暨監管溝通交流會

掃描識別圖中二維
查看詳細信息

03
優美莫司涂層冠狀動脈球囊擴張導管獲批上市
掃描識別圖中二維碼
查看詳細信息

藥典委
1. 本周發布海馬萬應膏國家藥品標準草案的公示。
掃描識別圖中二維碼
查看詳細信息

-END-



轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
