政策法規||復方藥物臨床試驗技術指導原則(征求意見稿)(附本周法規概覽09.05-09.09)
01
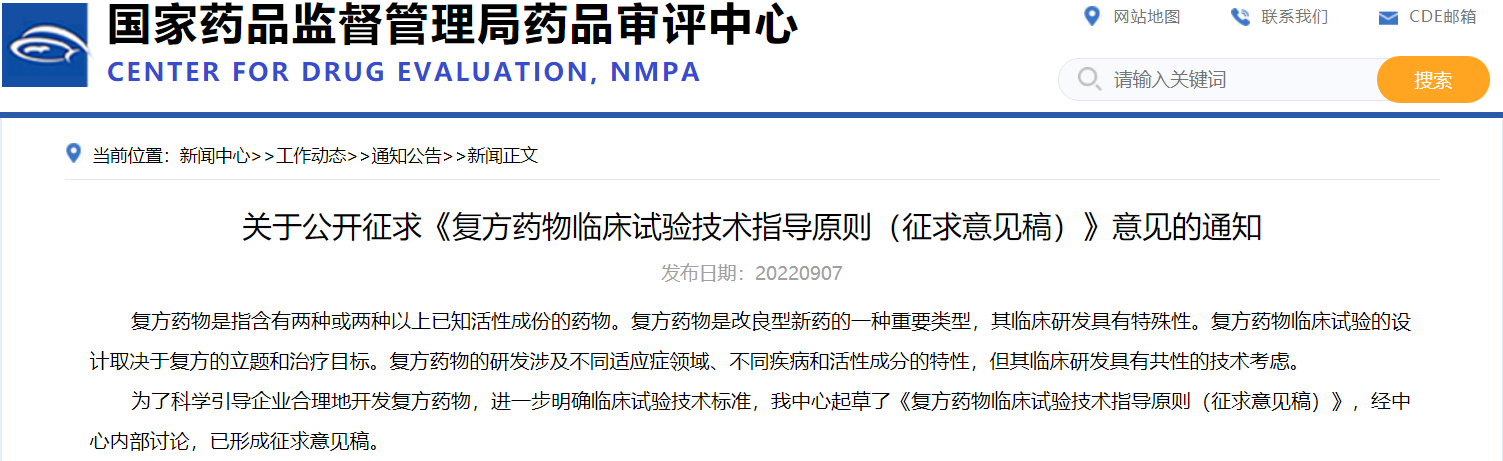
《關于公開征求《復方藥物臨床試驗技術指導原則(征求意見稿)》意見的通知》
復方藥物是指含有兩種或兩種以上已知活性成份的藥物。復方藥物是改良型新藥的一種重要類型,其臨床研發具有特殊性。復方藥物臨床試驗的設計取決于復方的立題和治療目標。復方藥物的研發涉及不同適應癥領域、不同疾病和活性成分的特性,但其臨床研發具有共性的技術考慮。為了科學引導企業合理地開發復方藥物,進一步明確臨床試驗技術標準,國家藥品監督管理局藥品審評中心起草《復方藥物臨床試驗技術指導原則(征求意見稿)》。
掃描識別圖中二維碼
查看詳細信息

01
關于公開征求《阿片類口服固體仿制藥防濫用藥學研究技術指導原則(征求意見稿)》意見的通知

掃描識別圖中二維碼
查看詳細信息

02
關于公開征求ICH《Q3D(R2):元素雜質指導原則》實施建議和中文版的通知

掃描識別圖中二維碼
查看詳細信息

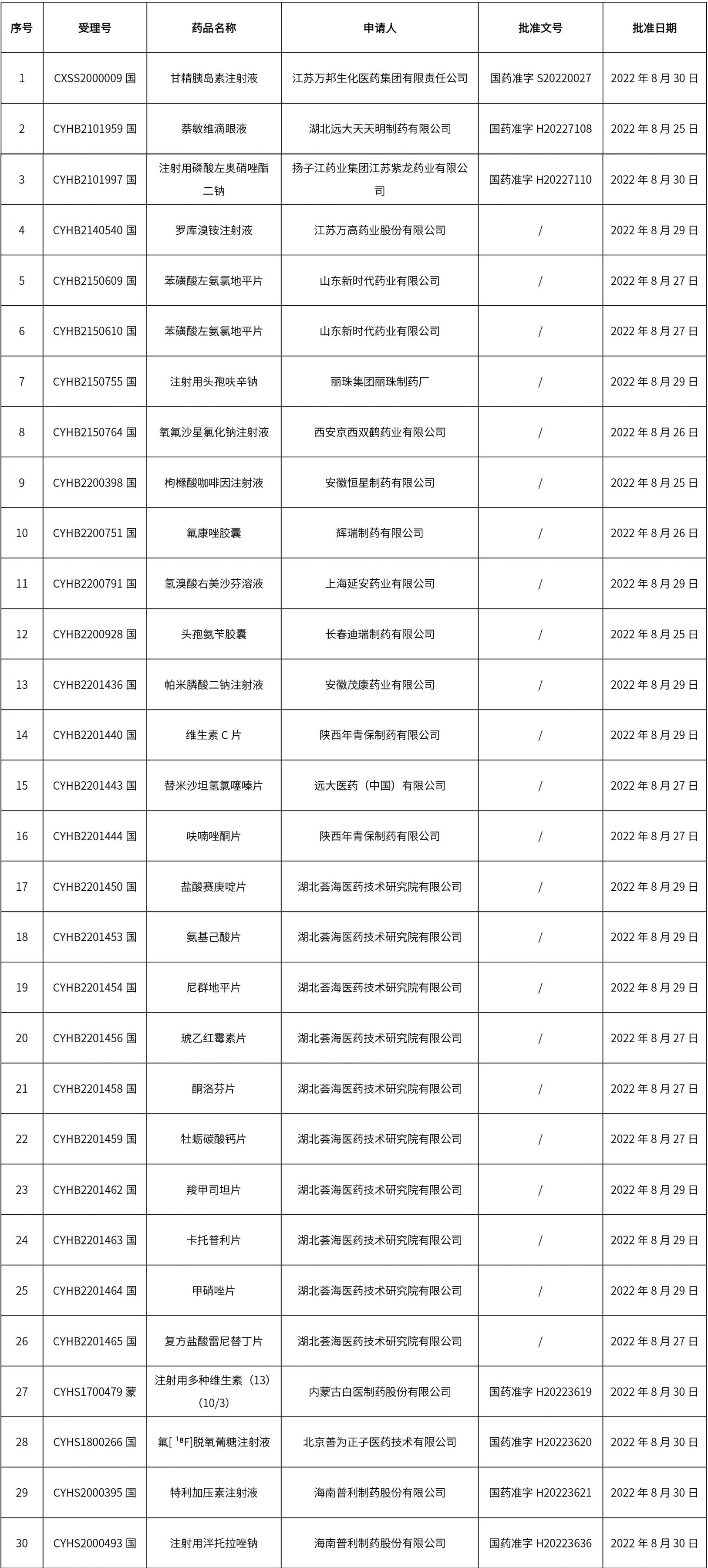
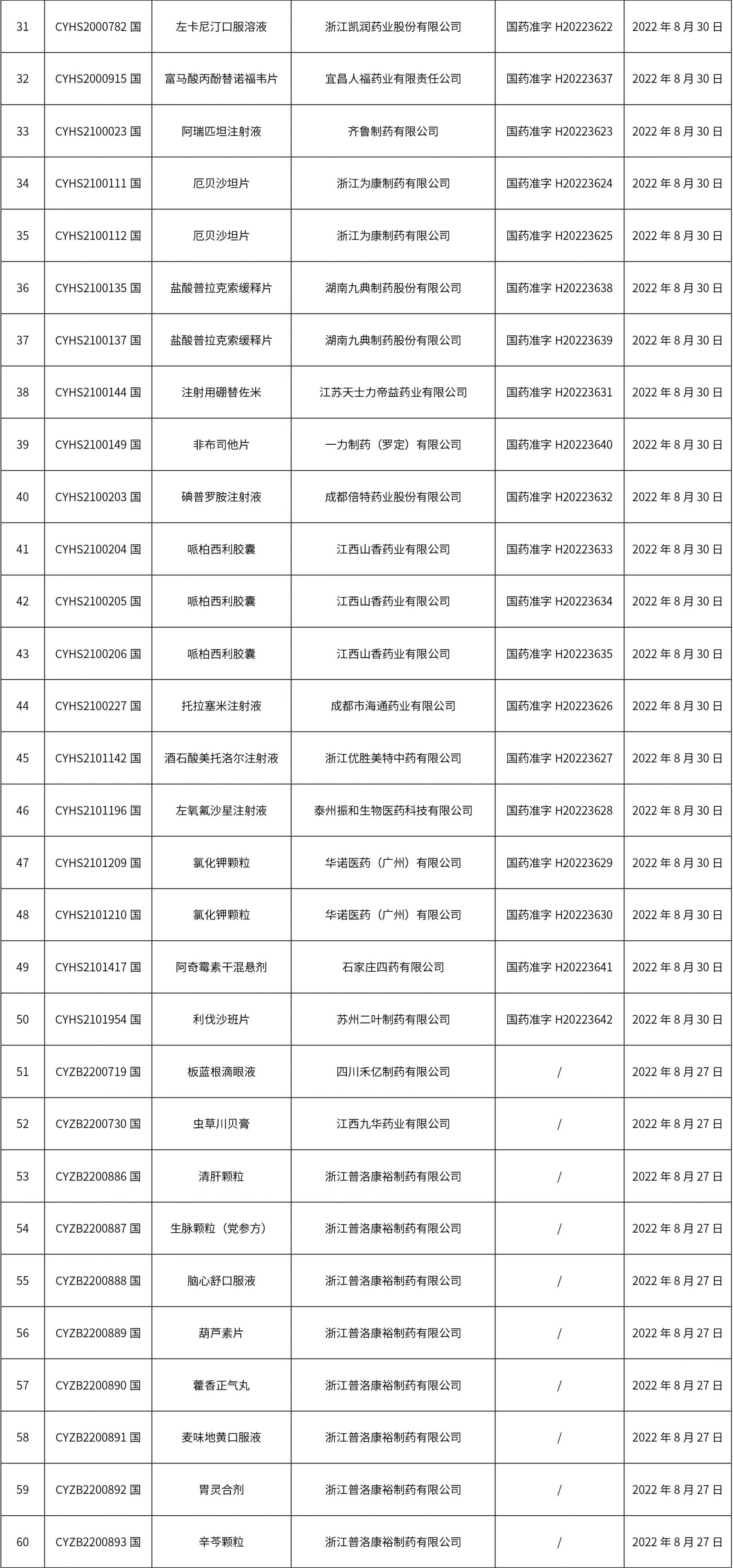
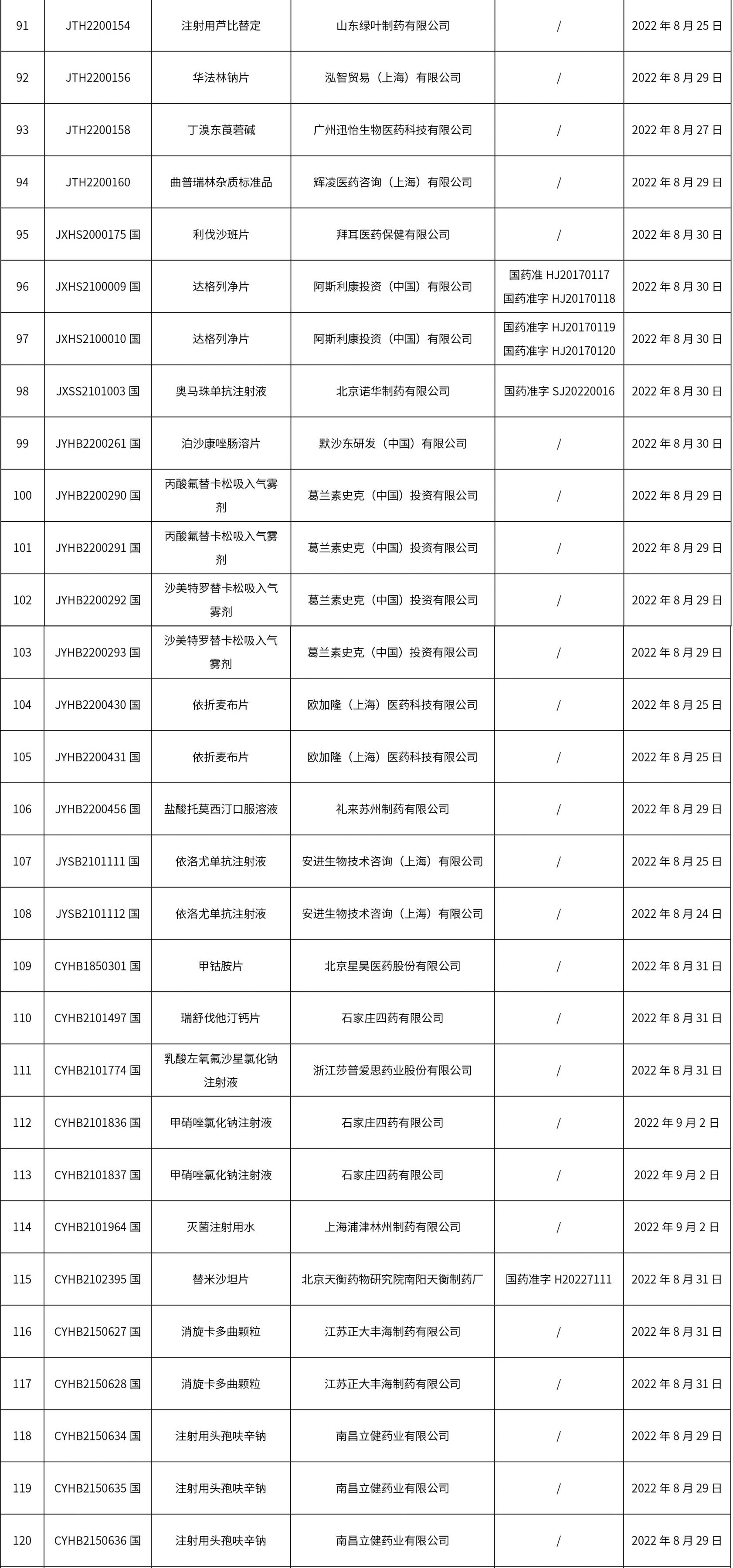
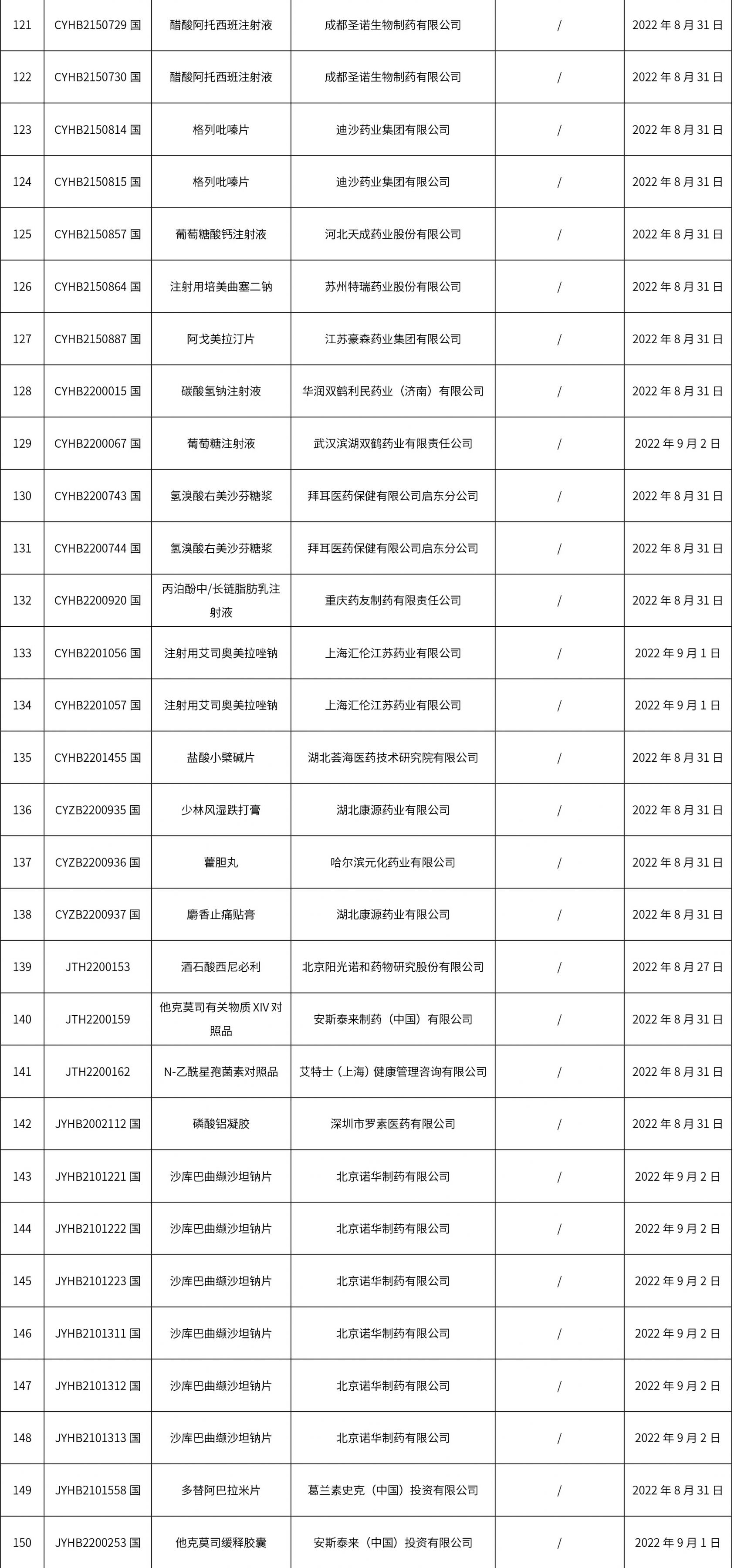
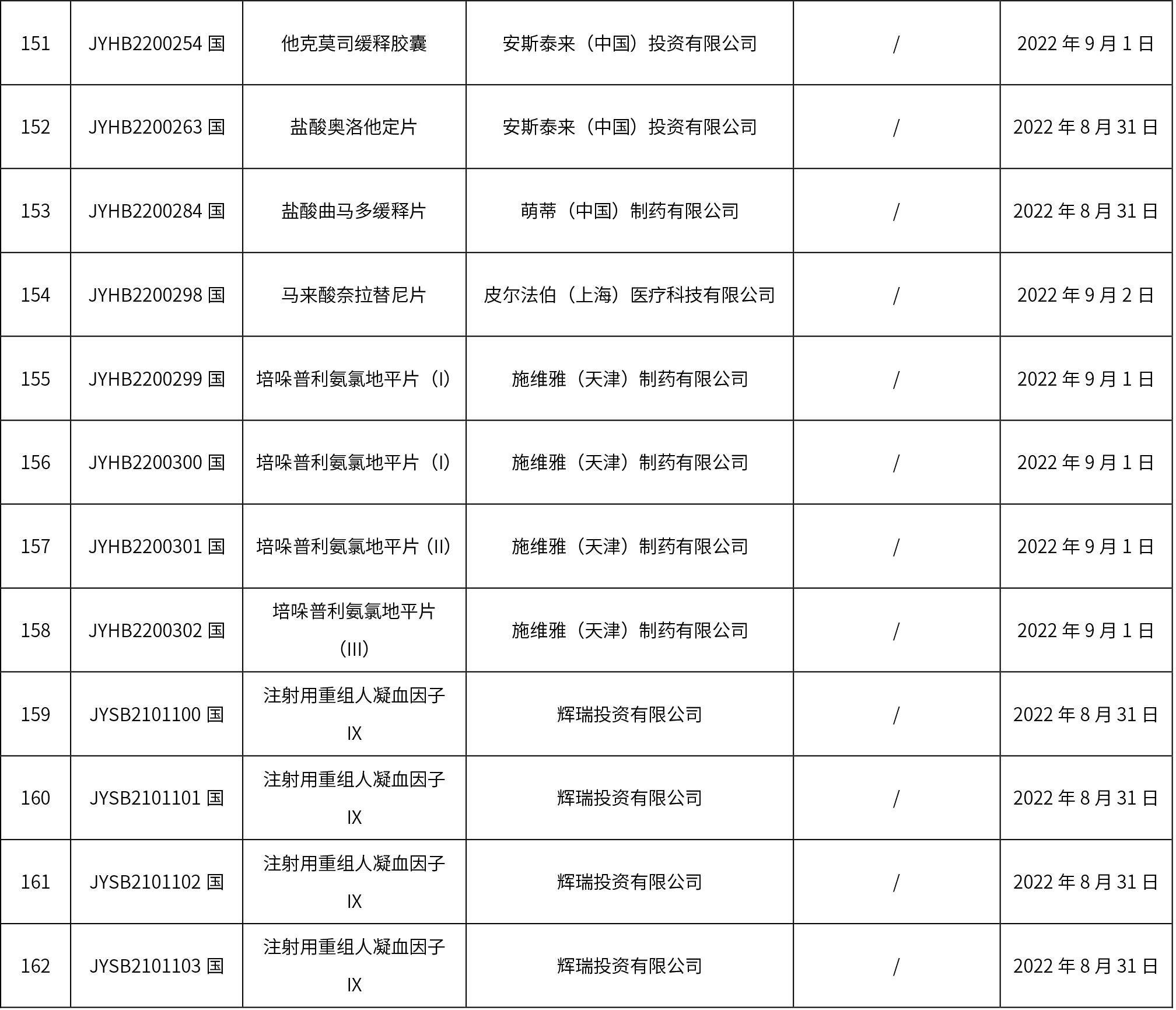
1. 本周(截止到9月9日12:35)共發布了162個品規的藥品批準證明文件待領取信息,其中一致性評價18個,注射劑41個。

02
國家藥監局關于啟用藥品、醫療器械產品注冊費電子繳款書的通告(2022年第37號)
掃描識別圖中二維碼
查看詳細信息

03
國家藥監局關于鼓勵企業和社會第三方參與中藥標準制定修訂工作有關事項的公告(2022年第70號)
掃描識別圖中二維碼
查看詳細信息

04
國家藥監局關于修訂羥乙基淀粉類注射劑說明書的公告(2022年第72號)
掃描識別圖中二維碼
查看詳細信息

01
關于舉辦2022年第二期藥物臨床試驗注冊核查交流會的通知

掃描識別圖中二維碼
查看詳細信息

02
北京市藥品審評檢查中心啟動藥物臨床試驗機構GCP符合性檢查
長按識別圖中二維碼
查看詳細信息

1. 本周藥典委發布13個品種國家藥品標準草案的公示。
掃描識別圖中二維碼
查看詳細信息

-END-



轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
