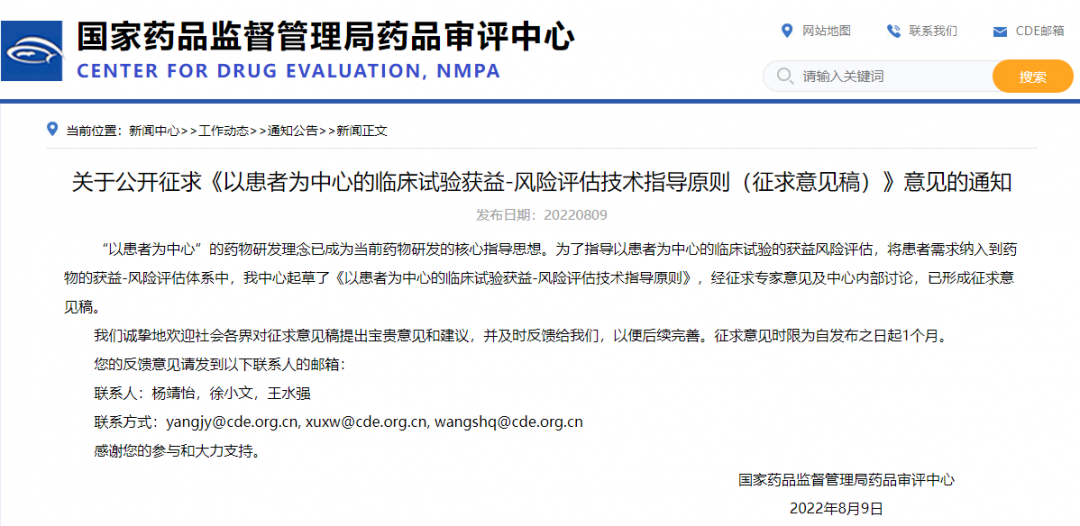
關于公開征求《以患者為中心的臨床試驗獲益-風險評估技術指導原則(征求意見稿)》意見的通知
政策法規||《以患者為中心的臨床試驗獲益-風險評估技術指導原則(征求意見稿)》(附法規概覽08.01-08.12)
01
關于公開征求《原發性膽汁性膽管炎治療藥物臨床試驗技術指導原則》意見的通知
為進一步規范和指導原發性膽汁性膽管炎治療藥物臨床試驗,提供可參考的技術規范,我中心起草了《原發性膽汁性膽管炎治療藥物臨床試驗技術指導原則。

長按識別圖中二維碼
查看詳細信息

02
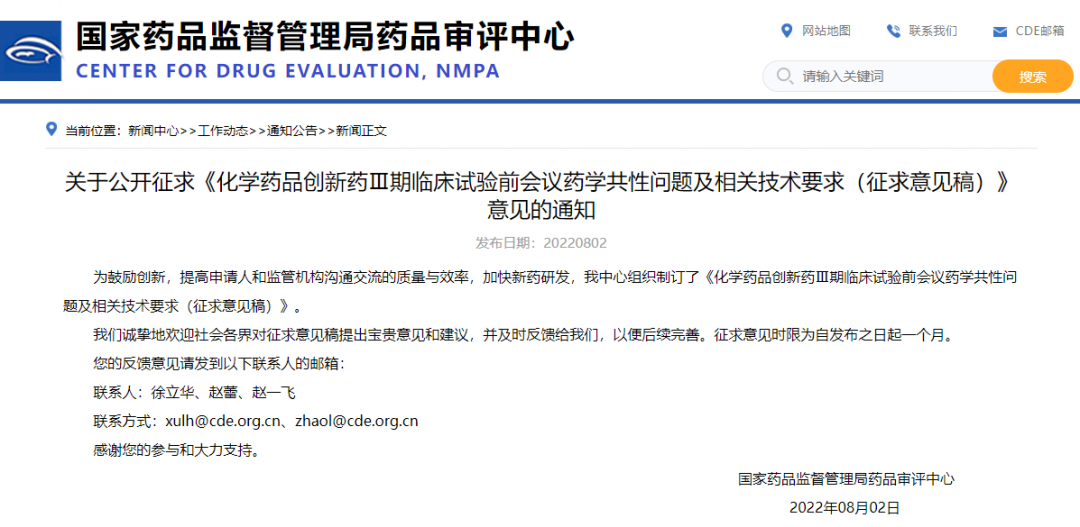
關于公開征求《化學藥品創新藥Ⅲ期臨床試驗前會議藥學共性問題及相關技術要求(征求意見稿)》意見的通知
長按識別圖中二維碼
查看詳細信息

03
“以患者為中心”的藥物研發理念已成為當前藥物研發的核心指導思想。為了指導以患者為中心的臨床試驗的獲益風險評估,將患者需求納入到藥物的獲益-風險評估體系中,我中心起草了《以患者為中心的臨床試驗獲益-風險評估技術指導原則》,經征求專家意見及中心內部討論,已形成征求意見稿。
長按識別圖中二維碼
查看詳細信息

04
關于公開征求《以患者為中心的臨床試驗設計技術指導原則(征求意見稿)》意見的通知
“以患者為中心”的藥物研發是指以患者需求為出發點、視患者為主動參與者、以臨床價值為最終目的,該理念已成為當前藥物研發的核心指導思想。為了指導以患者為中心的臨床試驗的設計,即不斷了解患者需求,在符合科學性的原則下將有意義的患者體驗數據納入臨床試驗設計要素的考量中,并充分關注受試者的感受,我中心起草了《以患者為中心的臨床試驗設計技術指導原則(征求意見稿)》,旨在闡明以患者為中心的臨床試驗的一般原則、整體研發計劃、以患者為中心的臨床試驗設計要素和其他考量,為臨床試驗設計提供指引和參考。經中心內部討論,已形成征求意見稿。

長按識別圖中二維碼
查看詳細信息

05
關于公開征求《以患者為中心的臨床試驗實施技術指導原則》(征求意見稿)意見的通知
“以患者為中心”的藥物研發是指以患者需求為出發點、視患者為主動參與者、以臨床價值為最終目的,該理念已成為當前藥物研發的核心指導思想。為了實施更加患者可及、友好、便利的臨床試驗,藥品審評中心組織起草了《以患者為中心的臨床試驗實施技術指導原則》的征求意見稿。我們誠摯歡迎社會各界對征求意見稿提出寶貴意見和建議,并及時反饋給我們,以便后續完善。征求意見時限為自發布之日起1個月。

長按識別圖中二維碼
查看詳細信息

NMPA
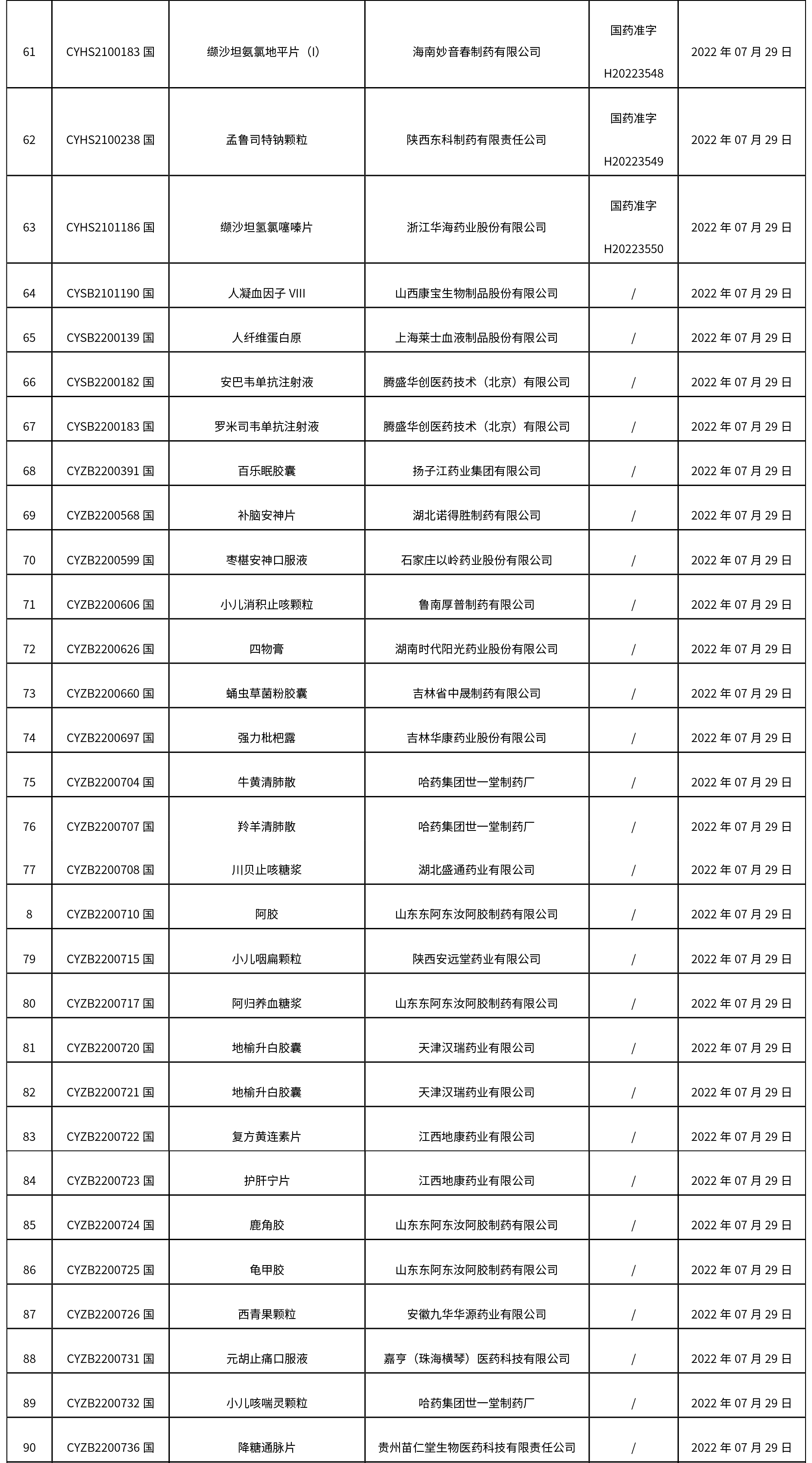
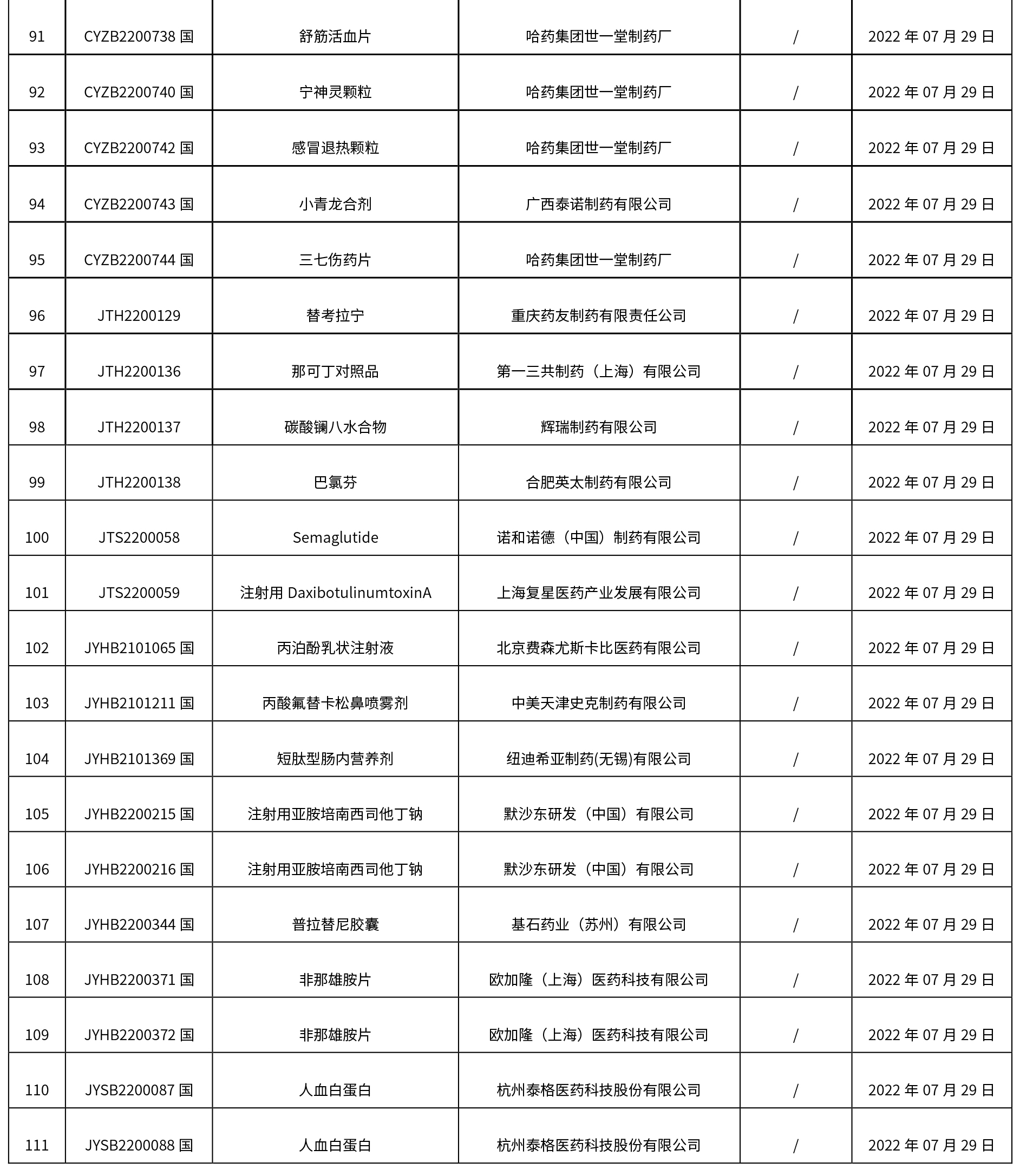
1. 本周(截止到8.12下午4:00)共計111個品種取得藥品批準證明文件,其中一致性評價品種5個。
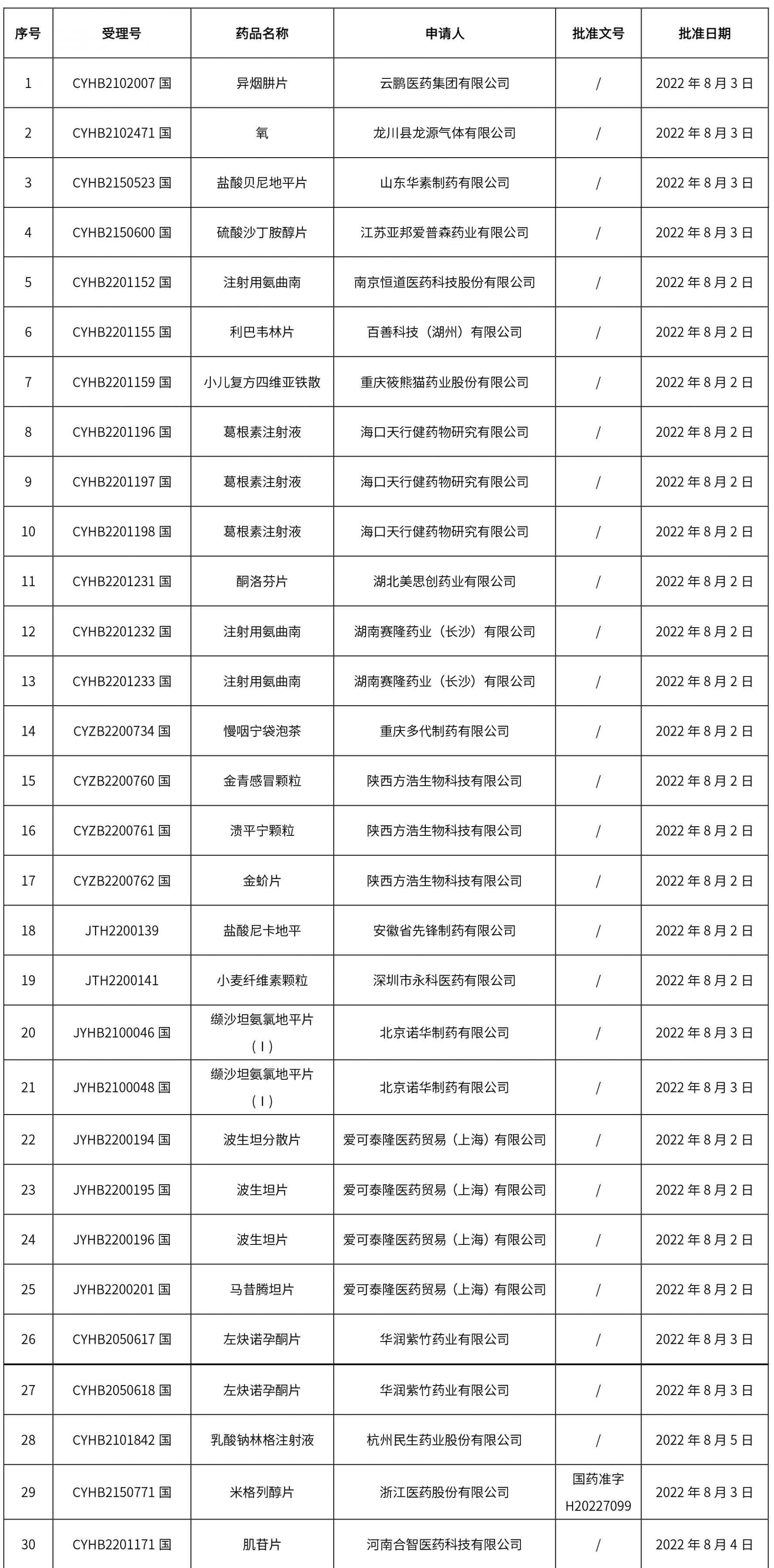
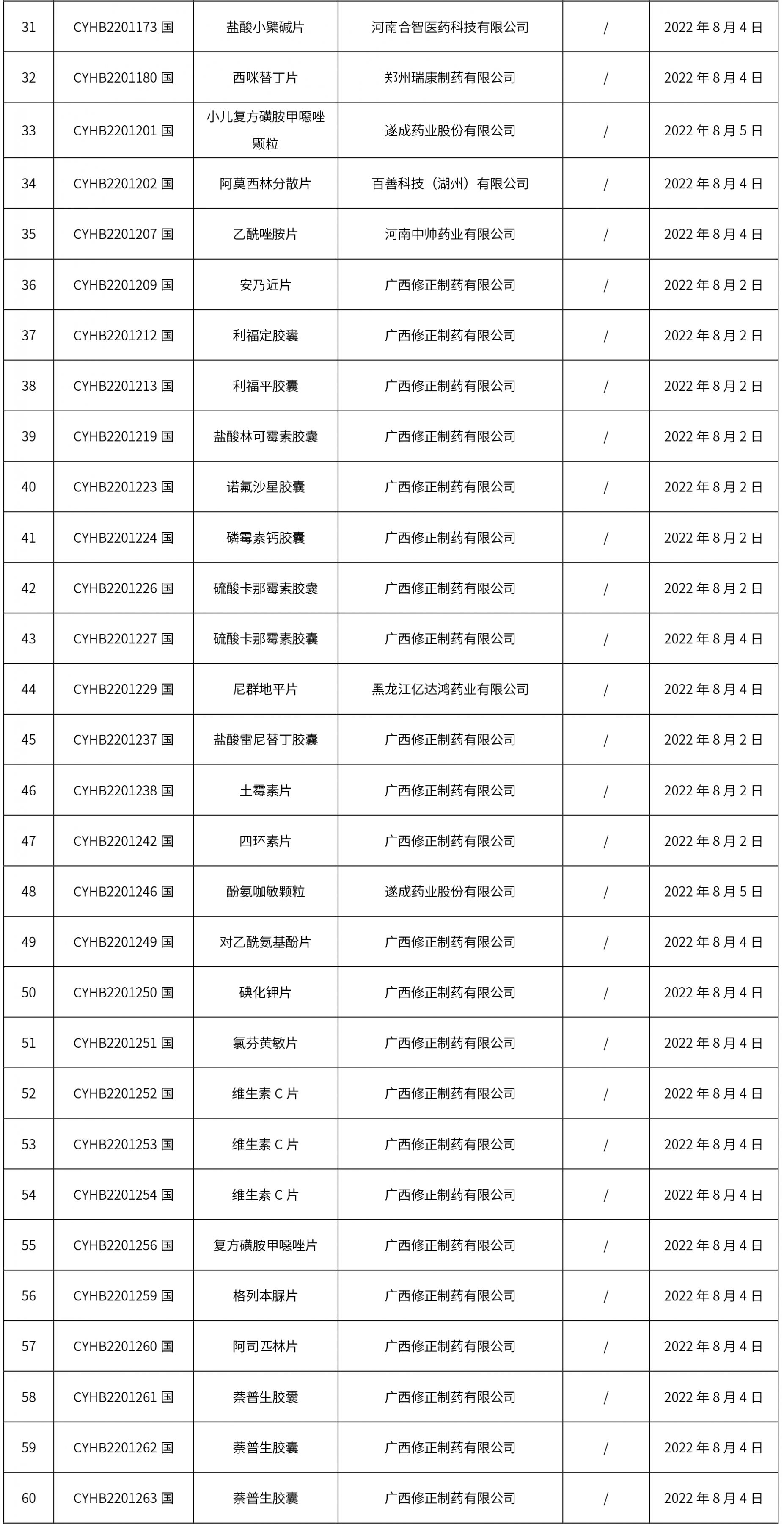
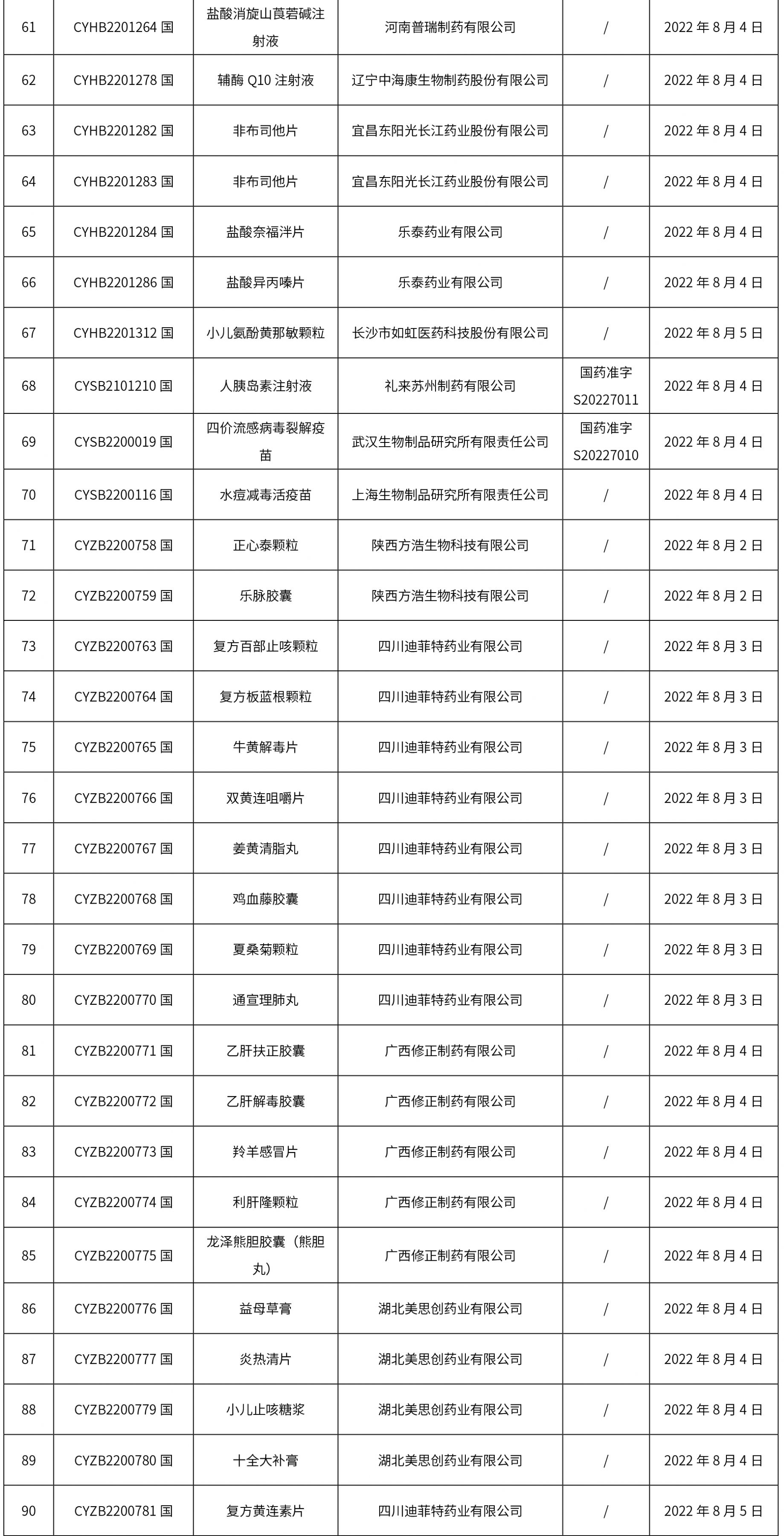
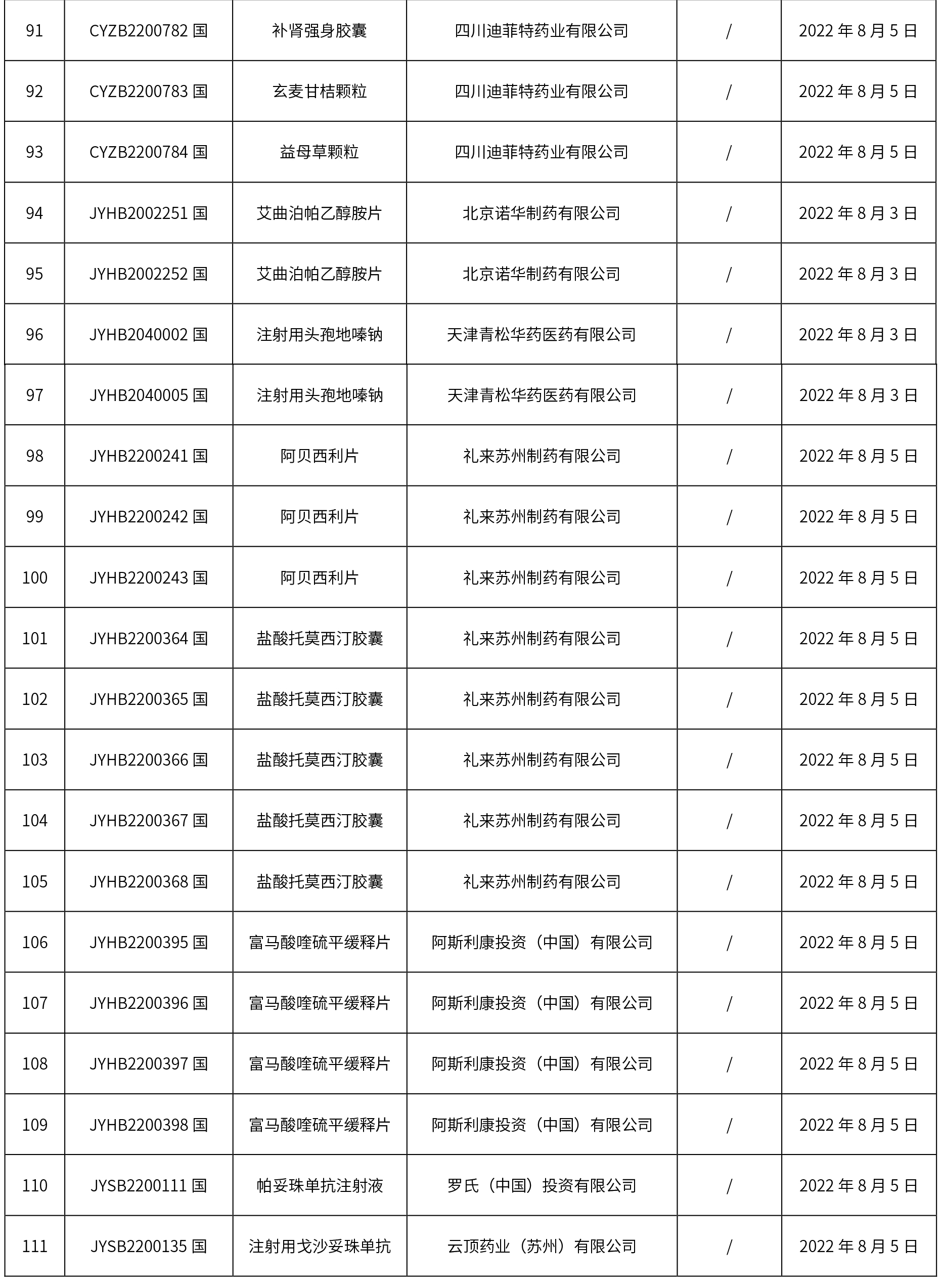
2.0 本周共發布了111個品規的藥品批準證明文件待領取信息,其中一致性評價10個,注射劑48個。
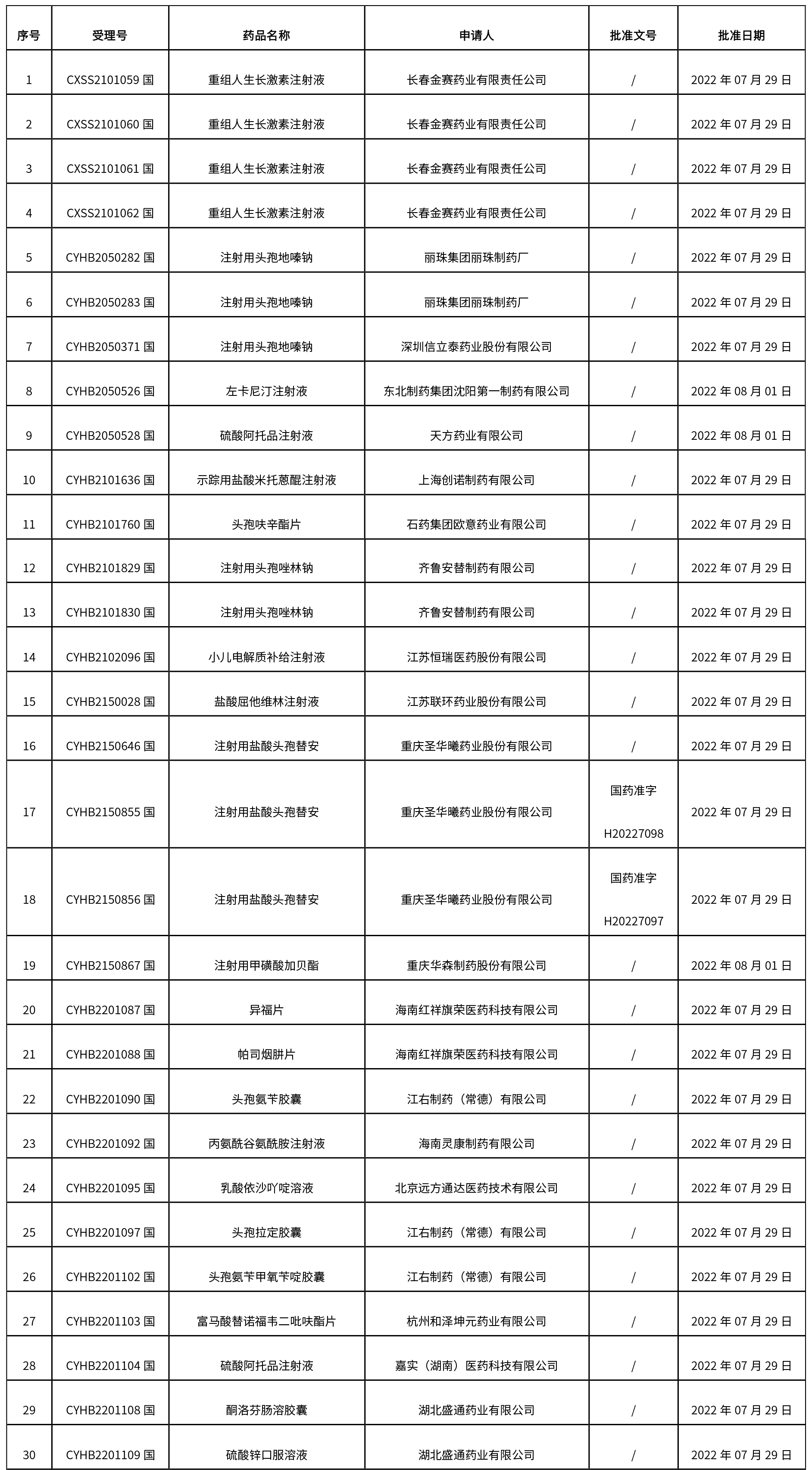
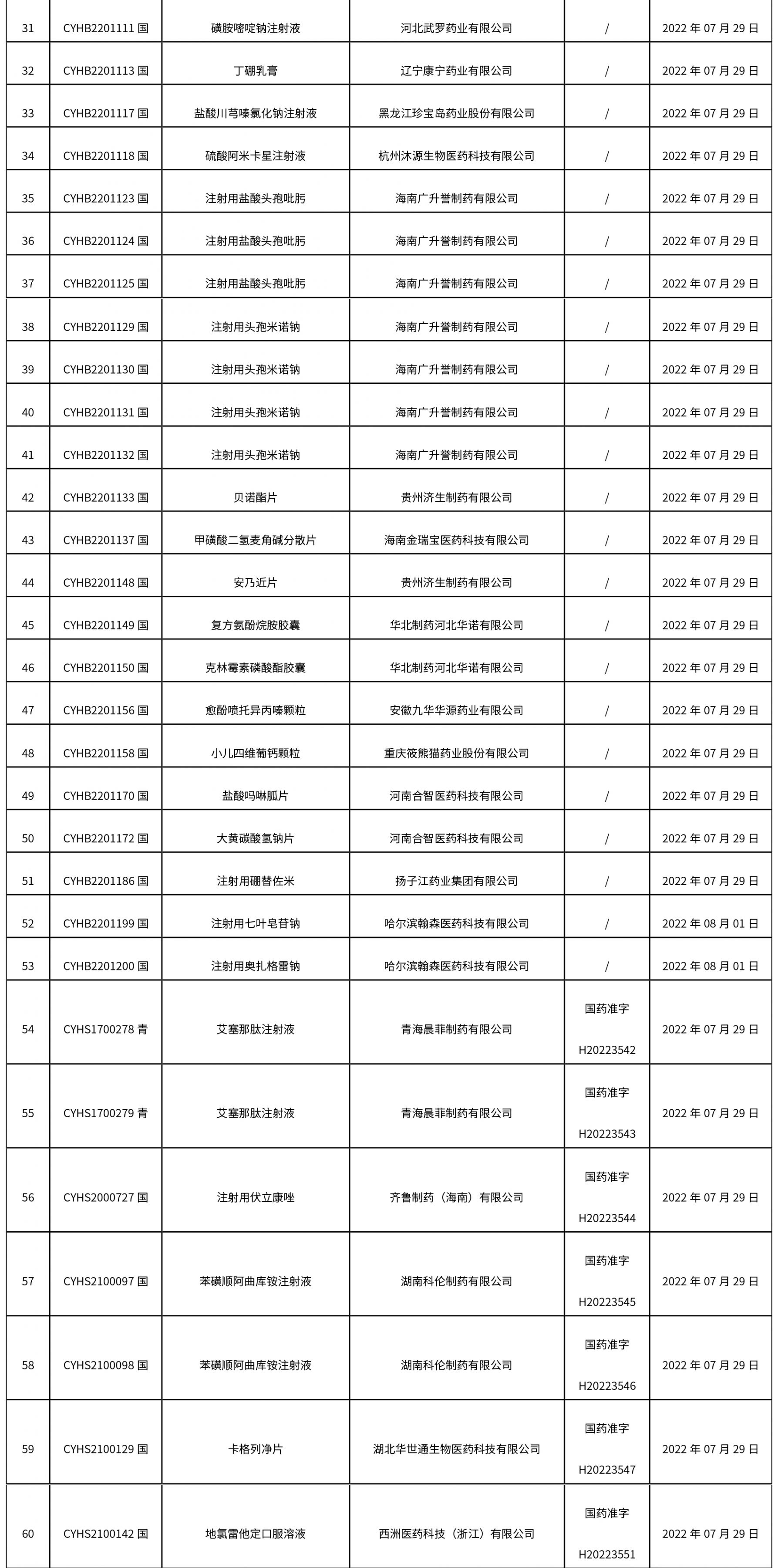
藥典委
長按識別圖中二維碼
查看詳細信息

-END-



轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
