指南 | 凝膠貼膏劑處方工藝開發技術標準及流程
本文旨在探討凝膠貼膏劑處方工藝開發技術標準和流程,主要內容包括處方前研究、小試處方工藝研究、小試放大等。
01 原料藥
-
制劑生產商需結合制劑質量的要求,根據國內外相關指導原則和國內外藥典標準,對原料藥的質量進行充分研究與評估,制定合理的內控標準,以保證制劑的質量。
-
應對可能影響制劑性能及生產可行性的原料藥的理化及生物特性進行研究,特別是影響遞送速率的性質,如分子量、熔點、分配系數、pKa、溶解性能和pH值等。
-
原料藥的其他特性,如粒度分布、晶型與晶型穩定性等,應根據產品性能進行評估和論證,如對于原料藥以混懸形式存在于制劑產品中,應對其晶型、粒度分布等加以充分研究及控制,以使仿制品達到和參比制劑的質量一致。
- 應重點考察原料對光、熱、濕、氧、酸堿等的穩定性情況。
02 輔料與材料
-
輔料種類(Q1)及用量(Q2)盡量與參比制劑保持一致,可能涉及生物等效性是否豁免。
-
輔料應符合現行版中國藥典要求。中國藥典未收載的輔料可按美、歐、日等藥典標準加以要求。國內外藥典均未收載的非關鍵性外用藥輔料,可以參考化妝品、食品標準制定相應的符合藥用要求的內控標準。
-
凝膠貼膏劑所使用的輔料與材料可能包括凝膠骨架、促滲劑、增溶劑、增塑劑、增黏劑、保濕劑、充填劑、抗氧劑、抑菌劑、交聯劑、交聯調節劑、結晶抑制劑、背襯材料、保護層等。研究者應根據輔料與材料的特性以及在制劑中的用途,對輔料與材料(特別是可能影響藥物黏附性、滲透性及生物利用度的輔料與材料)的功能性相關指標進行研究,并在物料內控標準中予以體現。
-
對某些大分子聚合物等關鍵性輔料,應結合其修飾基團種類、數量、聚合度、分子量分布、熔點/熔距等特性指標加以控制,同時對批次、供應商等可能會影響質量的因素也應予以關注。
-
對于黏合劑(壓敏膠),應根據其用途考慮以下屬性:
黏合劑自身性質:分子量、多分散性、光譜分析、熱分析、特性或復合黏度、以及殘余單體、二聚體、溶劑、重金屬、催化劑和引發劑。
終產品(制劑)中黏合劑:鑒別、殘留單體、二聚體和溶劑。應評估黏合劑中可能包含殘留的單體、引發劑副產物、醛等化合物的安全性,對于任何具有毒理學意義的雜質應制定控制策略。
-
膜性材料 應根據其不同用途進行相關研究,如背襯材料、保護層等應對外觀、柔韌性、抗拉強度、孔隙率、密封性(Occlusion)、化學惰性等特性進行研究。
對生產過程中使用但最終去除的物料(如臨時膜材、溶劑等)進行必要的研究,評估上述物料組分轉移并殘留至終產品中所導致的質量及安全性風險。
03 標識
-
標簽標識一般印在貼劑的背襯層上,至少應包括產品名稱和規格。
-
對于管制類藥物,應根據監管要求,確保在貼劑的全生命周期均具有足夠的對比度和辨識度,可采用機械模擬試驗(如摩擦等)與化學模擬試驗(如噴淋、洗滌劑清洗等)來考察標識持久性。
-
應對標簽標識的印刷材料與貼劑之間的相互作用進行研究,以評估其對貼劑的質量及安全性的影響。
04 原輔料相容性
對于外用半固體制劑,目前無原輔料相容性的相關指導原則,建議采用類似固體制劑的二元混合物進行考察,即各輔料分別與原料藥物理混合形成二元混合物,采用影響因素條件(高溫、高濕、強光照)放樣10天或30天,以外觀性質、吸濕增重、有關物質等作為考察指標。
05 參比制劑研究
對比參比制劑進行質量研究、反向剖析及穩定性考察,具體如下。

小試處方工藝研究
01 基本思路
凝膠貼膏劑小試處方工藝篩選的基本思路為:先以常規項(性狀、pH、含量、有關物質等)、顯微特性(顯微狀態、晶型、粒度)、物理特性、流變學特性、黏附性等為考察指標,與參比制劑一致后,再以IVRT、IVPT為考察指標,最終達到自制品Q3與參比制劑一致。
另外,穩定性為處方工藝考察的關鍵指標,需同步考察。處方工藝開發階段穩定性考察實驗包括:離心試驗、耐寒/耐熱試驗、影響因素試驗(高溫、高濕、光照、低溫、凍融等)、加速試驗。
離心試驗非常快速有效,主要用于快速評估制劑物理穩定性,為首推的穩定性評估方法,離心參數通常可選擇轉速5000-8000rpm、時間5min,離心轉速和時間可以根據實際情況進行優化。
耐寒試驗:-15℃放置24h。
耐熱試驗:55℃放置6h。
小試處方工藝確定的標準:原則上要求0天質量全檢合格以及至少1個月穩定性(影響因素、加速試驗)結果符合要求。
02 小試處方研究
-
基本原則
一般認為,凝膠貼膏仿制藥的輔料種類(Q1)和用量(Q2)應與參比制劑基本一致,會有助于保證仿制藥與參比制劑質量的一致性。故建議研究者通過查閱參比制劑說明書、專利、文獻及適當的處方解析手段,對參比制劑的處方進行分析,并在此基礎上對處方進行科學、合理的開發,以使仿制品與參比制劑的輔料種類及用量盡可能一致。
如有充分的依據證明仿制藥與參比制劑的 Q1 和Q2 一致,且質量也一致( Q3) 的情況下,可基于國外先進監管機構對該具體品種的生物等效性指南(如 FDA 發布的Guidance on Acyclovir Cream)的相關要求,申請豁免人體試驗。
-
處方篩選
首先參考參比制劑說明書、原研專利等,設計預處方,對預處方進行質量評估,然后在預處方的基礎上對輔料用量、原輔料來源等進行考察,具體如下:
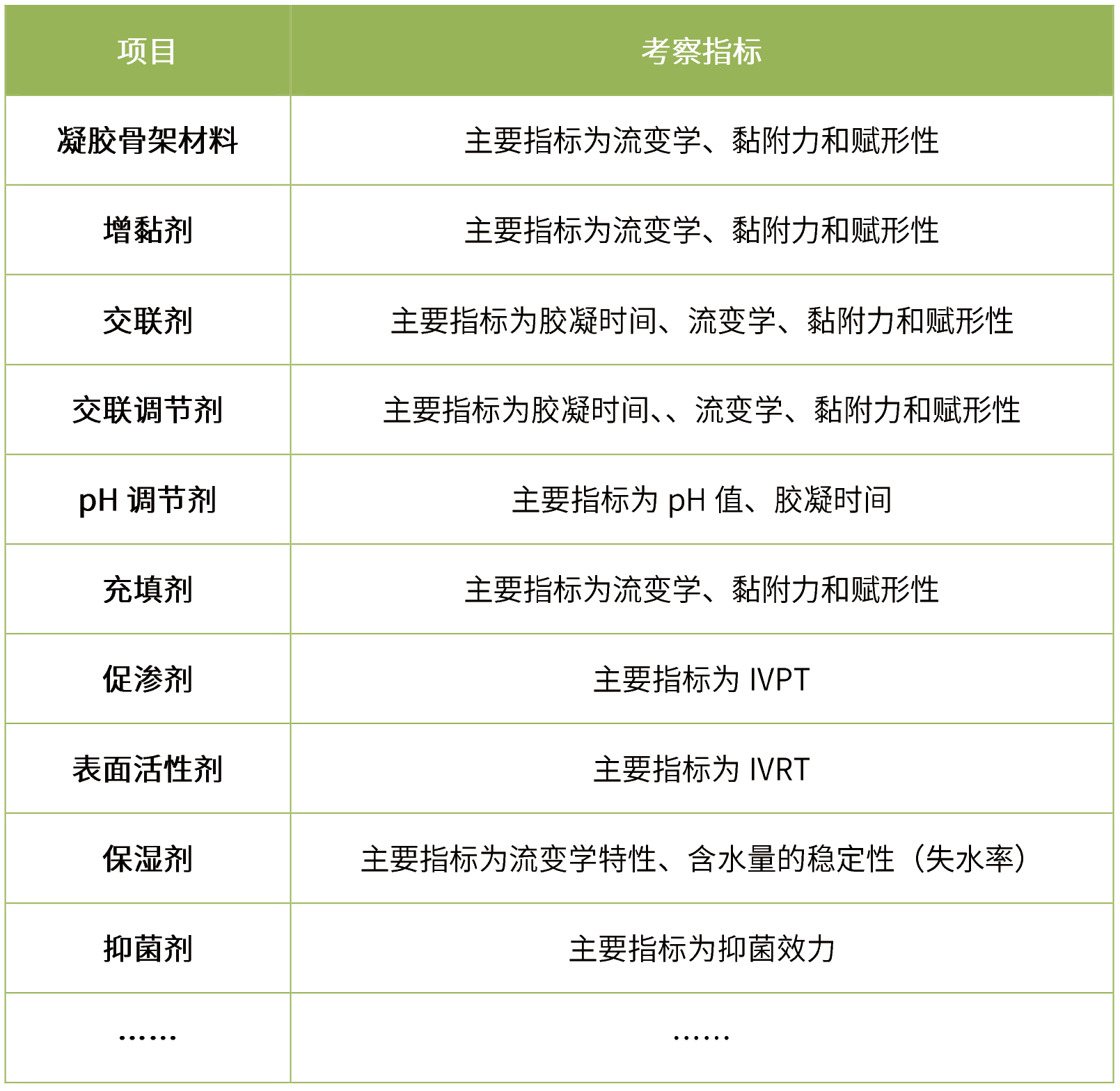
-
材料/包材考察
在參比材料與包材剖析的基礎上,考察材料和包材型號、來源對制劑的影響,具體如下:
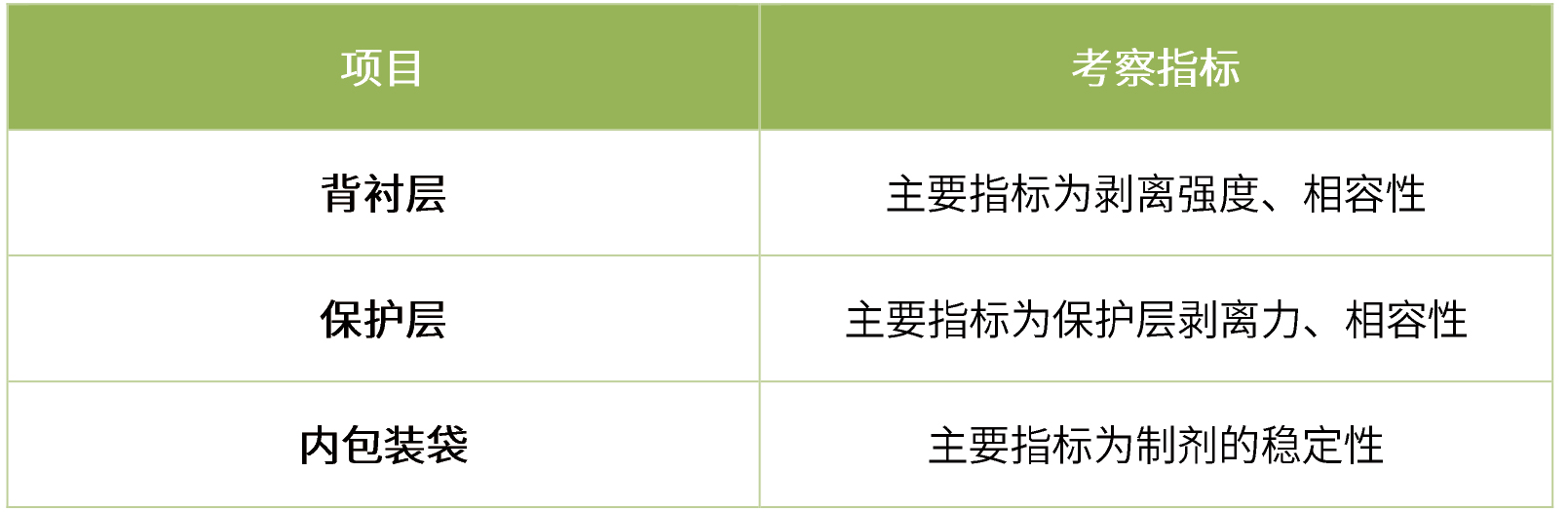
-
材料/包材相容性
提取物:應在藥物開發過程中進行可提取物的研究,以了解擬定商業化成品中可能存在的可浸出物。這些研究應考察從背襯材料、保護層、印刷油墨、包裝材料等除藥物和黏合劑基質以外的成分中提取出來的化合物。在提取物研究中需說明提取溶劑選擇的合理性,使用的提取溶劑應包括擬定商業化處方中的已知殘留溶劑。
浸出物:應對臨床極端情況下(如劇烈運動出汗)的可浸出物進行研究。應對溶劑、溫度、攪拌程度、接觸溶劑的時間等試驗條件進行合理選擇。
03 小試工藝研究
凝膠貼膏劑主要生產工序包括:稱量、制膏、涂布/裁切、包裝、入庫等。實驗室小試工藝研究包括但不局限于以下內容:
-
制膏工藝:一般需要對加料順序、配制溫度、攪拌速度、攪拌時間、真空度等參數進行考察。
1)加料順序:包括水相(A相)加料順序、油相(B相加料順序)、兩相混合順序,加料順序對工藝過程及制劑質量影響顯著,需重點考察,主要考察指標為制膏時間、性狀、顯微特性、流變學特性、黏附力和賦形性等。
加料順序考察需關注點如下:
a.遵循相似相溶的原則
b.親水凝膠骨架材料(如聚丙烯酸鈉)及高分子親水增稠劑(如羧甲基纖維素鈉)不易直接加在純水中溶解,因為該類高分子材料在純水中易結團導致溶解困難,一般可采用醇水溶液進行溶解(如甘油水溶液、丙二醇水溶液等)
2)配制溫度:配制溫度主要影響物料的溶解或分散速度,需重點考察,凝膠貼膏劑的配制溫度一般在室溫至40℃,需要根據物料的實際溶解情況進行考察確認。主要考察指標為制膏時間、性狀、顯微特性、流變學特性、黏附力和賦形性等。
3)攪拌速度和攪拌時間:攪拌速度和攪拌時間影響物料的溶解或分散,需重點考察,主要考察指標為制膏時間、性狀、顯微特性、流變學特性、黏附力和賦形性等。
4)真空度:兩相物料混合后一般需要在真空條件下(如-0.08MPa)進行混合或乳化,以除去膏體中的空氣,使膏體均勻細膩,主要考察指標為性狀、顯微特性、流變學特性等。
-
涂布/裁切: 涂布/裁切工序主要需考察膠凝時間、涂布速度,主要指標為含膏量、涂布厚度、含量、含量均勻度、裁切面積差異、重量差異等。
膠凝時間是指混合均勻后形成不能從容器中倒出的凝膠所需的時間,故需要在凝膠時間內完成涂布工序。
-
制備過程是否避光: 考察制膏及涂布過程是否需要避光,主要指標為性狀、有關物質等。
小試處方工藝確定后,進行實驗室小試放大,批次至少為3批。小試放大各工序均要采用相應小試設備,主要關注點包括但不局限于以下:
-
在小試放大設備上對關鍵工藝參數進行優化,以及考察工藝耐用性,做好中間體的控制,重點關注放大效應。
-
對小試放大樣品進行全面質量研究,包括常規項(性狀、含膏量、水分、含量、含量均勻度、有關物質、pH等)、顯微特性(顯微狀態、晶型、粒度等)、流變學特性、賦形性、冷流、黏附力(初黏力、持黏力、剝離強度、黏著力)、IVRT、IVPT等,各質量屬性應與參比制劑一致。
-
對小試放大樣品進行初步穩定性考察,主要包括影響因素試驗(含低溫、凍熔試驗)、加速試驗和長期試驗、使用過程穩定性等。
-END-
關于我們:
透皮給藥制劑平臺由原空軍總后特色醫學中心少將、新領先副總裁顏耀東先生帶領團隊創建,同時聘請中國藥科大學教授、大連理工大學教授等多位專家作為平臺技術顧問,平臺致力于解決透皮給藥制劑的技術壁壘、提高產品的質量和療效,為國內外提供透皮給藥制劑藥學及臨床服務的專業研發平臺。
平臺研發團隊20余人,均來自國內外一流大學,從事醫藥研發10余年。平臺可開展化藥外用洗劑、凝膠劑、膏劑、貼劑等劑型的研究,同時能夠提供臨床研究、注冊服務等服務。
目前,平臺已經開展了多個化藥外用仿制制劑及兩個2類新藥外用制劑的研發工作。


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
