政策法規||本周重磅政策法規概覽(21.05.17-21.05.21)
NMPA/CDE/CFDI/藥典委公布藥品相關內容本周集錦。
01
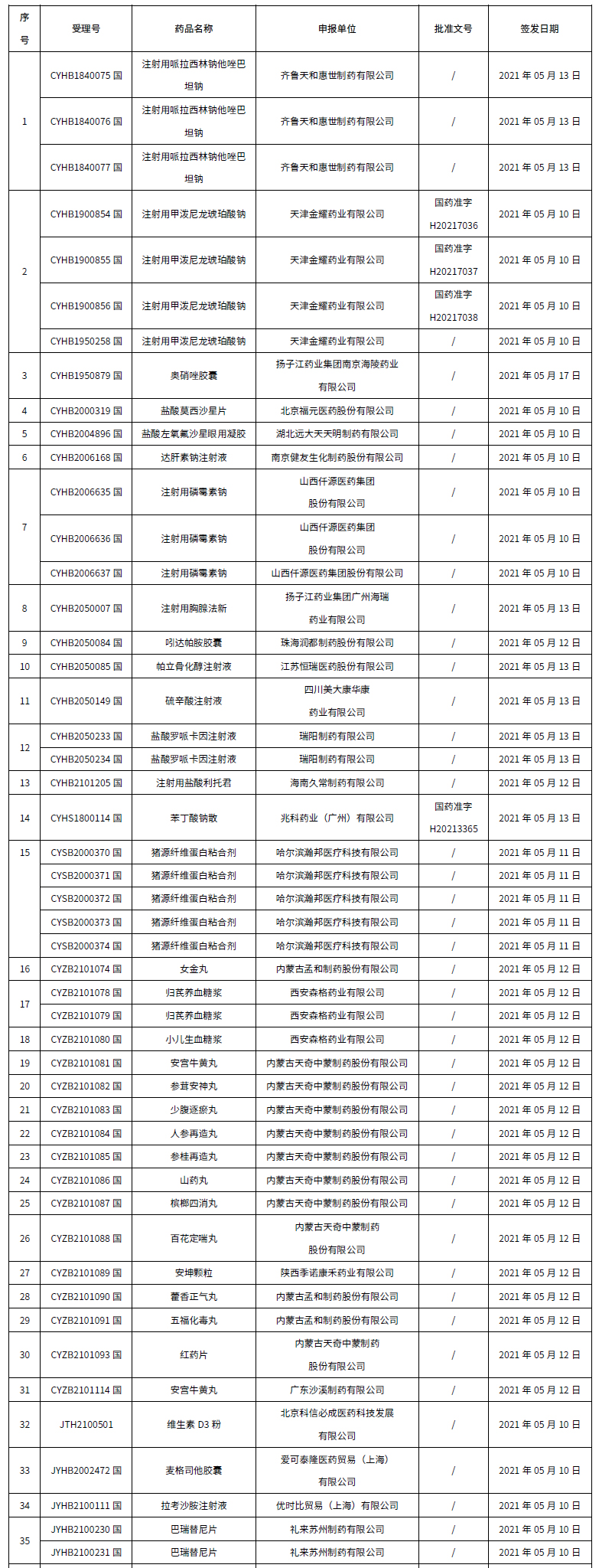
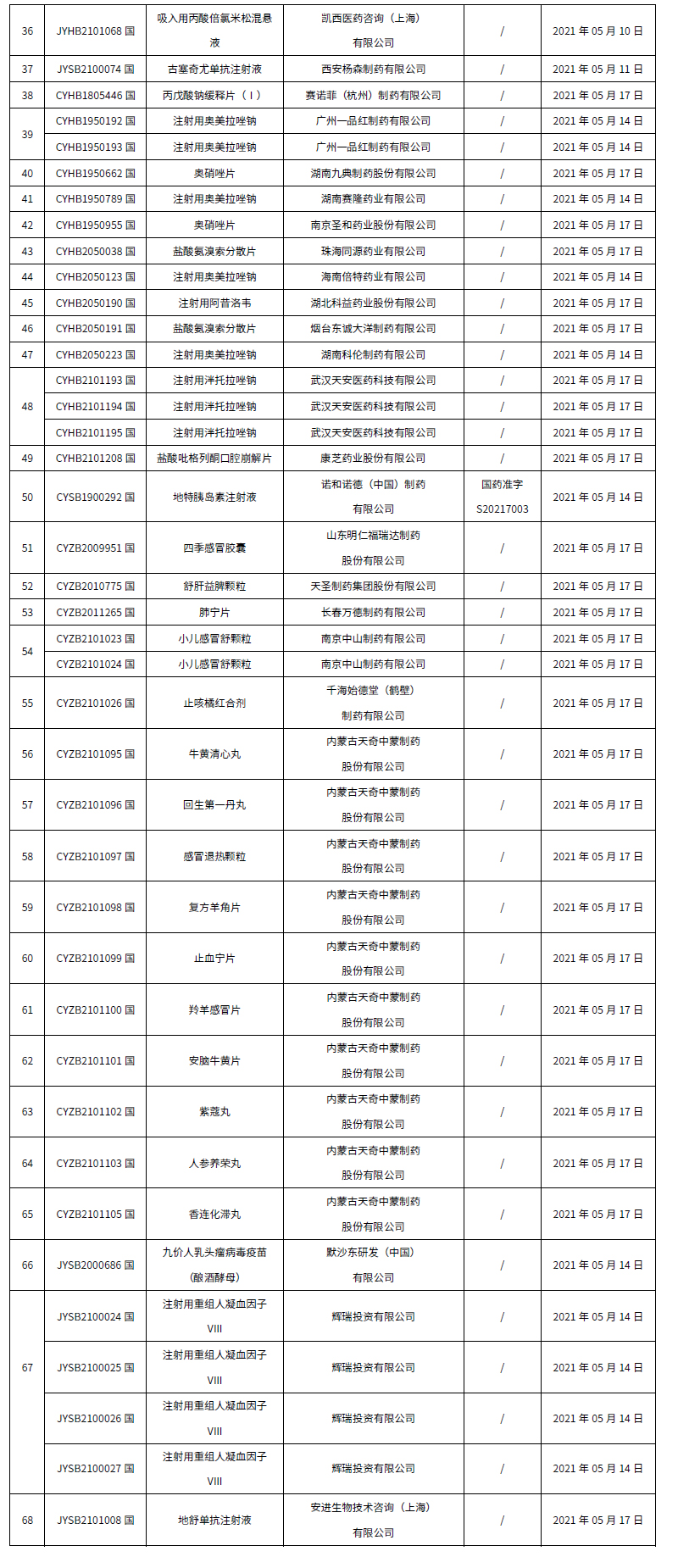
本周共計68個品種獲批取得藥品批準證明文件,其中一致性評價品種17個,包括注射劑品種11個。
國家藥監局關于修訂銀杏達莫注射液說明書的公告(2021年第71號)
一、本品的上市許可持有人應依據《藥品注冊管理辦法》等有關規定,按照銀杏達莫注射液說明書修訂要求(見附件),提出修訂說明書的補充申請,于2021年8月19日前報國家藥品監督管理局藥品審評中心或省級藥品監管部門備案。修訂內容涉及藥品標簽的,應當一并進行修訂;說明書及標簽其他內容應當與原批準內容一致。在備案之日起生產的藥品,不得繼續使用原藥品說明書。藥品上市許可持有人應當在備案后9個月內對所有已出廠的藥品說明書及標簽予以更換。
二、藥品上市許可持有人應當對新增不良反應發生機制開展深入研究,采取有效措施做好使用和安全性問題的宣傳培訓,涉及用藥安全的內容變更要立即以適當方式通知藥品經營和使用單位,指導醫師、藥師合理用藥。
三、臨床醫師、藥師應當仔細閱讀銀杏達莫注射液說明書的修訂內容,在選擇用藥時,應當根據新修訂說明書進行充分的獲益/風險分析。
四、患者用藥前應當仔細閱讀說明書,應嚴格遵醫囑用藥。
五、省級藥品監督管理部門應當督促行政區域內本品的藥品上市許可持有人按要求做好相應說明書修訂和標簽、說明書更換工作,對違法違規行為依法嚴厲查處。
掃描下方二維碼
查看詳細信息

01
關于發布《化學仿制藥參比制劑目錄(第四十三批)》的公示(征求意見稿)
本批公布共計40個品規的參比制劑來源;并且44個品種未通過審議,原因主要集中于安全有效性數據有限、經評價不具有參比制劑地位、規格不符合國內用法用量、擬申請參比制劑與已發布參比制劑濃度相同僅裝量不同、改劑型未改變給藥途徑且無明顯臨床優勢等。

掃描下方二維碼
查看詳細信息

關于發布《化學仿制藥參比制劑目錄(第四十四批)》的公示(征求意見稿)
本批公布共計59個品規的參比制劑來源,其中新增補40個;并且30個品種未通過審議,原因主要集中于原研進口參比制劑且可獲得,擬申請參比制劑為美國或日本上市的仿制藥、缺乏完整充分的安全有效性數據等。

掃描下方二維碼
查看詳細信息

關于藥品專利糾紛早期解決機制相關專利信息登記平臺公開測試等有關事宜的通知
為貫徹落實《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》以及《專利法》有關規定,國家藥監局會同有關部門積極推進藥品專利糾紛早期解決機制實施辦法的制定和出臺。為配合辦法實施,根據國家藥監局整體工作部署,經內部討論和征詢專家及相關部門意見,我中心搭建了中國上市藥品專利信息登記平臺,并附填表說明、專利聲明公開模板。現對登記平臺開展公開測試,并征集各方意見。

掃描下方二維碼
查看詳細信息

藥品審評檢查長三角分中心及大灣區分中心開始啟動藥品注冊核查工作
2021年5月17日,國家藥監局核查中心指導藥品審評檢查長三角分中心開始了首家藥品注冊生產現場核查。5月8日,藥品審評檢查大灣區分中心也已啟動了首家藥品注冊核查。
核查中心就藥品注冊核查有關工作與藥品審評檢查長三角分中心及大灣區分中心開展進行了數次全面、充分的溝通交流。根據分中心實際情況,核查中心全程指導其建立了各類藥品注冊核查工作程序與標準。結合兩個分中心對其當前資源與能力評估情況,將第一批9個位于長三角地區及5個位于大灣區的藥品注冊核查任務轉對應分中心組織開展。核查中心對核查全過程進行指導,并協調國家藥品檢查員參與支持。相關任務調整事宜國家藥監局核查中心已正式發文通知相關藥品注冊申請人。
掃描下方二維碼
查看詳細信息

本周去乙酰毛花苷、纈沙坦片、纈沙坦膠囊、吡拉西坦注射液、復方爐甘石眼膏、鶴蟾片國家藥品標準草案公示;纈沙坦國家藥品標準修訂草案的公示;烏梅炭、蛇蛻、瓜蔞皮、丁香、決明子、炒決明子、萊菔子、蒲黃、生馬錢子、鹽菟絲子、菟絲子、水蛭、葶藶子、芫花、九香蟲、炒九香蟲全國中藥飲片炮制規范品種草案公示。
掃描下方二維碼
查看詳細信息

-END-
關于我們:
藥政部是隸屬于公司副總裁直接領導下的部門,以國家藥品政策為導向,以為客戶提供集藥物研發、注冊申報、現場核查等一體化專業技術服務為宗旨,以高效、成功申報項目最終目標。
藥政部擁有一支技術與注冊經驗豐富的團隊,作為一家提供專業服務的公司,在原料藥登記、仿制藥一致性評價、仿制藥注冊、新藥注冊以及進口藥品注冊等方面均具有專業且豐富的經驗,已助力成功申報多項藥品注冊申請,在業內具有良好的口碑。
部門堅持 “忠誠、思考、建設、承擔、分享”的公司理念,不斷加強人才隊伍建設、提升專業能力、豐富注冊經驗、拓展業務范圍,致力于為客戶提供高效率、高質量、合規的技術服務,為保護和促進公眾健康而不懈努力。


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
