政策法規(guī)||本周重磅政策法規(guī)概覽(20.11.23-11.27)
NMPA/CDE/CFDI/藥典委公布藥品/醫(yī)療器械相關(guān)內(nèi)容本周集錦。
?
NMPA
?
01
?
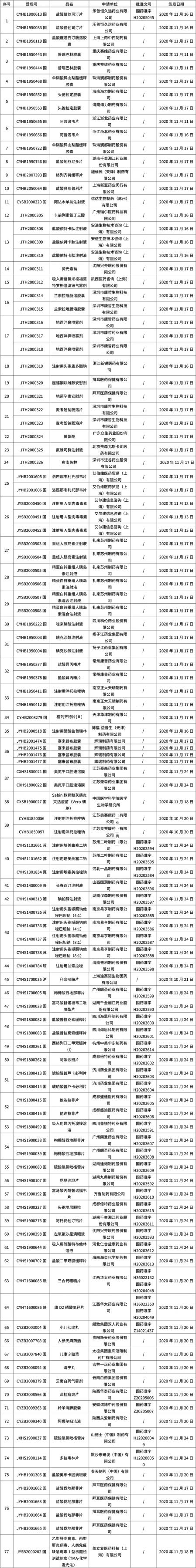
本周共計(jì)77+53個(gè)品種獲批取得藥品批準(zhǔn)證明文件(特殊藥品批文53個(gè)),其中一致性評(píng)價(jià)品種12個(gè)。
?
?
02
?
關(guān)于發(fā)布仿制藥參比制劑目錄(第三十一批)、(第三十二批)的通告
?
兩批次共計(jì)202個(gè)品規(guī)參比制劑來源公布,其中頭孢呋辛酯片、利丙雙卡因乳膏等因持證商名稱或通用名稱變更公示。
?

掃描下方二維碼
查看詳細(xì)信息

?

掃描下方二維碼
查看詳細(xì)信息

?
03
?
關(guān)于發(fā)布真實(shí)世界數(shù)據(jù)用于醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則(試行)的通告(2020年第77號(hào))
?
為規(guī)范和指導(dǎo)真實(shí)世界數(shù)據(jù)在醫(yī)療器械臨床評(píng)價(jià)中的應(yīng)用,該指導(dǎo)原則予以發(fā)布并執(zhí)行。
?

掃描下方二維碼
查看詳細(xì)信息

?
04
?
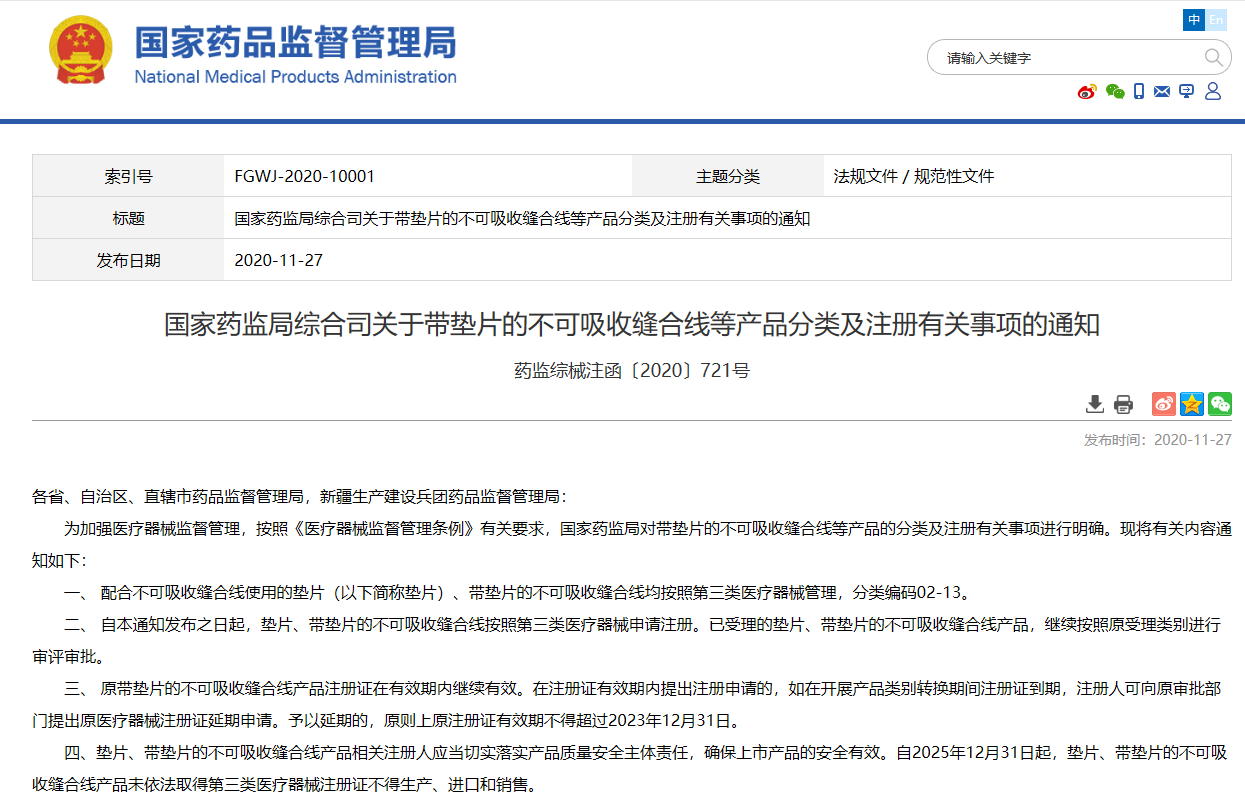
關(guān)于帶墊片的不可吸收縫合線等產(chǎn)品分類及注冊(cè)有關(guān)事項(xiàng)的通知 藥監(jiān)綜械注函〔2020〕721號(hào)
?
配合不可吸收縫合線使用的墊片(以下簡(jiǎn)稱墊片)、帶墊片的不可吸收縫合線均按照第三類醫(yī)療器械管理,分類編碼02-13。
?
掃描下方二維碼
查看詳細(xì)信息

?
CDE
?
01
?
關(guān)于發(fā)布《化學(xué)藥品創(chuàng)新藥I期臨床試驗(yàn)申請(qǐng)藥學(xué)共性問題相關(guān)技術(shù)要求》和《化學(xué)藥品I期臨床試驗(yàn)申請(qǐng)藥學(xué)研究信息匯總表(修訂版)》的通告(2020年第40號(hào))
?
藥審中心組織制定了《化學(xué)藥品創(chuàng)新藥I期臨床試驗(yàn)申請(qǐng)藥學(xué)共性問題相關(guān)技術(shù)要求》,同時(shí)對(duì)原食品藥品監(jiān)管總局《關(guān)于發(fā)布〈新藥I期臨床試驗(yàn)申請(qǐng)技術(shù)指南〉的通告》(2018年第16號(hào))中所附《化學(xué)藥品I期臨床試驗(yàn)申請(qǐng)藥學(xué)研究信息匯總表》進(jìn)行了修訂,并于11月12日起執(zhí)行。
?

掃描下方二維碼
查看詳細(xì)信息

?
02
?
關(guān)于公開征求《疫苗臨床試驗(yàn)抗體分析方法研究技術(shù)指導(dǎo)原則》意見的通知
?
為進(jìn)一步規(guī)范和指導(dǎo)疫苗臨床試驗(yàn)抗體分析的研究,該指導(dǎo)原則予以意見征求,時(shí)間截至至12月23日。
?

掃描下方二維碼
查看詳細(xì)信息

?
03
?
關(guān)于發(fā)布《藥品審評(píng)中心補(bǔ)充資料工作程序(試行)》的通告(2020年第42號(hào))
?
為進(jìn)一步規(guī)范藥品注冊(cè)審評(píng)補(bǔ)充資料管理工作,結(jié)合藥品審評(píng)以流程為導(dǎo)向的科學(xué)管理體系的研究成果和審評(píng)工作實(shí)際,該通告自12月1日起正式執(zhí)行,各申請(qǐng)人注意發(fā)補(bǔ)通知件中期限要求。
?

掃描下方二維碼
查看詳細(xì)信息

?
藥典委
?
本周奧沙拉秦鈉膠囊、阿膠益壽口服液、富馬酸替諾福韋二吡呋酯、卡培他濱片標(biāo)準(zhǔn)公示,及金銀花配方顆粒、熟地黃配方顆粒、淡竹葉配方顆粒、酒女貞子配方顆粒、淫羊藿配方顆粒、黃芪配方顆粒、炙淫羊藿配方顆粒、生地黃配方顆粒試點(diǎn)統(tǒng)一標(biāo)準(zhǔn)公示(第二次)。
?

掃描下方二維碼
查看詳細(xì)信息

?
-END-
?
關(guān)于我們:
?
? ? ? ?藥政部是隸屬于公司副總裁直接領(lǐng)導(dǎo)下的部門,以國(guó)家藥品政策為導(dǎo)向,以為客戶提供集藥物研發(fā)、注冊(cè)申報(bào)、現(xiàn)場(chǎng)核查等一體化專業(yè)技術(shù)服務(wù)為宗旨,以高效、成功申報(bào)項(xiàng)目最終目標(biāo)。
?
? ? ? ?藥政部擁有一支技術(shù)與注冊(cè)經(jīng)驗(yàn)豐富的團(tuán)隊(duì),作為一家提供專業(yè)服務(wù)的公司,在原料藥登記、仿制藥一致性評(píng)價(jià)、仿制藥注冊(cè)、新藥注冊(cè)以及進(jìn)口藥品注冊(cè)等方面均具有專業(yè)且豐富的經(jīng)驗(yàn),已助力成功申報(bào)多項(xiàng)藥品注冊(cè)申請(qǐng),在業(yè)內(nèi)具有良好的口碑。
? ? ? 部門堅(jiān)持 “忠誠(chéng)、思考、建設(shè)、承擔(dān)、分享”的公司理念,不斷加強(qiáng)人才隊(duì)伍建設(shè)、提升專業(yè)能力、豐富注冊(cè)經(jīng)驗(yàn)、拓展業(yè)務(wù)范圍,致力于為客戶提供高效率、高質(zhì)量、合規(guī)的技術(shù)服務(wù),為保護(hù)和促進(jìn)公眾健康而不懈努力。
?


轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務(wù)熱線:010-61006450
Hotline服務(wù)熱線:010-61006450
 簡(jiǎn)體中文
簡(jiǎn)體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場(chǎng)部:
技術(shù)市場(chǎng)部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
