政策法規(guī)||本周重磅政策法規(guī)概覽(21.01.04-01.08)
CDE/NMPA/CFDI/藥典委公布藥品/醫(yī)療器械相關(guān)內(nèi)容本周集錦。
關(guān)于發(fā)布《化學(xué)仿制藥參比制劑目錄(第三十八批)》的公示
本批公布共計31個品規(guī)的參比制劑來源,其中新增補(bǔ)27個;并且9個品種未通過審議,原因主要集中于本品原研不明,且其組方臨床價值不明;存在安全性風(fēng)險。

掃描圖中二維碼
查看詳細(xì)信息

NMPA
本周共計112+23+7個品種獲批取得藥品批準(zhǔn)證明文件,其中一致性評價品種46個。
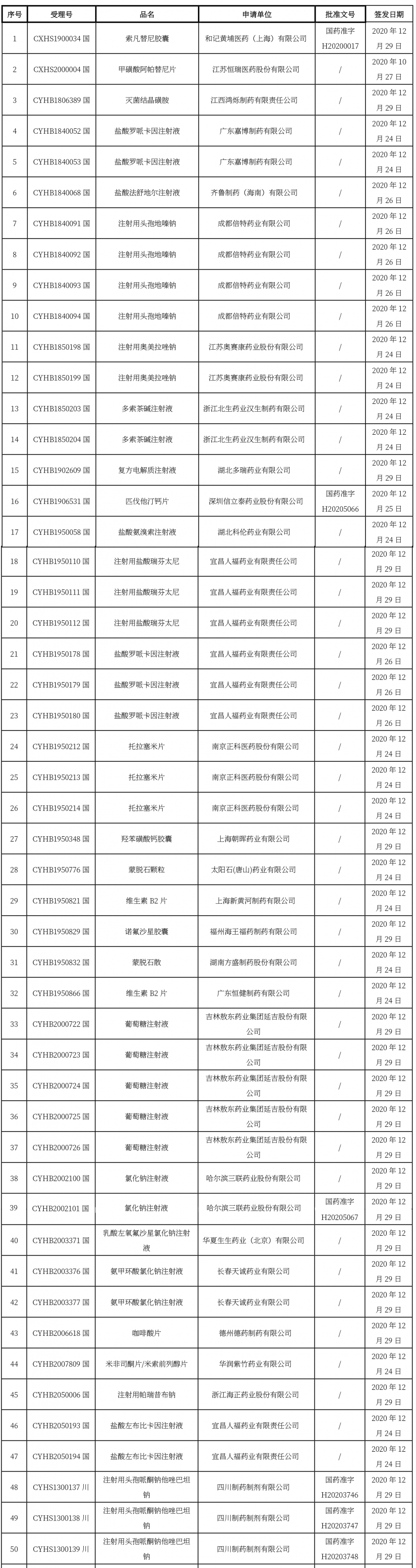
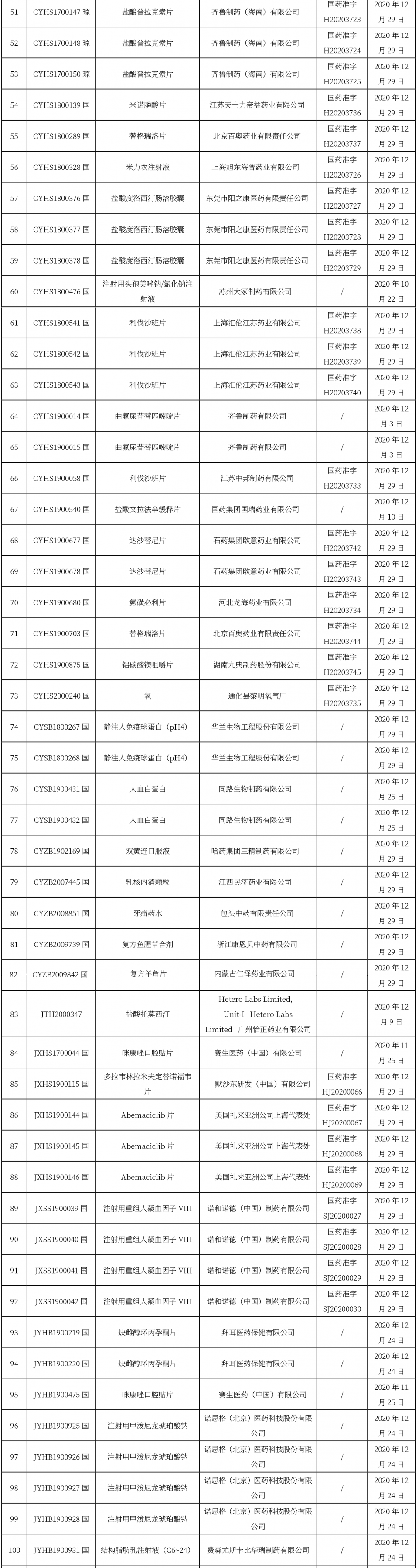
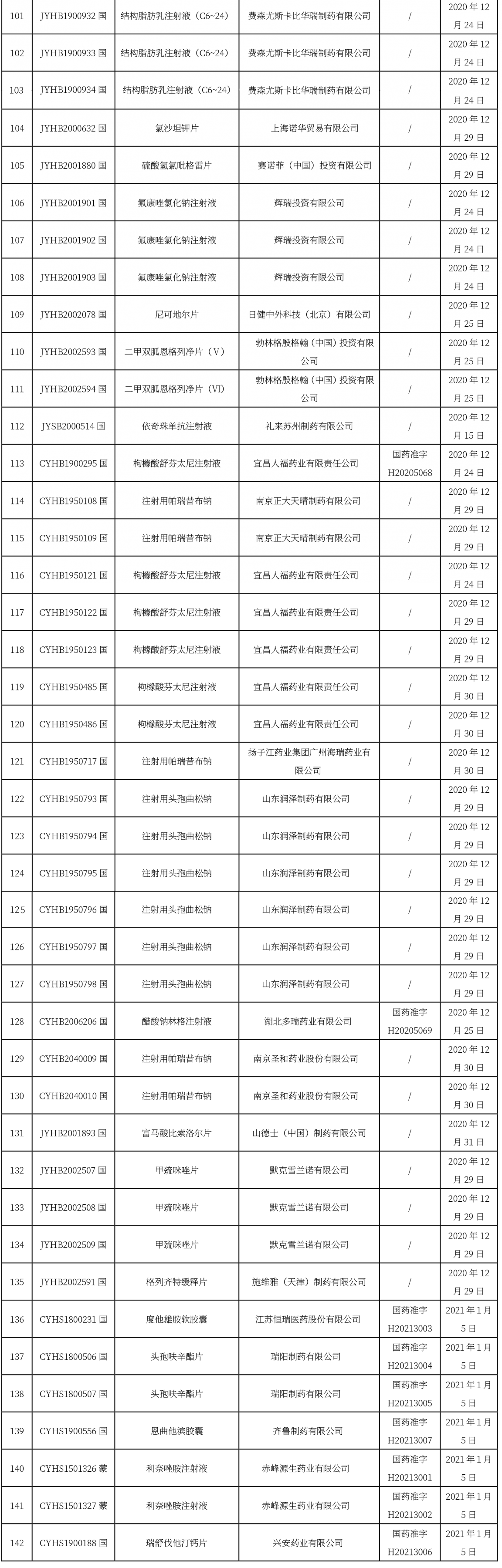
關(guān)于進(jìn)一步規(guī)范醫(yī)用超聲耦合劑說明書等有關(guān)內(nèi)容的公告(2020年第143號)
根據(jù)醫(yī)療器械風(fēng)險評價結(jié)果,為進(jìn)一步提升用械安全,消除風(fēng)險隱患,國家藥監(jiān)局決定進(jìn)一步規(guī)范醫(yī)用超聲耦合劑產(chǎn)品說明書及標(biāo)簽。

掃描圖中二維碼
查看詳細(xì)信息

2021年興奮劑目錄公告(第51號)
有關(guān)部門應(yīng)按照國務(wù)院《反興奮劑條例》的規(guī)定,做好2021年興奮劑目錄中所列物質(zhì)的生產(chǎn)、銷售、進(jìn)出口以及反對使用興奮劑的監(jiān)督管理工作。蛋白同化制劑和肽類激素的進(jìn)出口管理按照《蛋白同化制劑和肽類激素的進(jìn)出口管理辦法》(國家食品藥品監(jiān)督管理總局 海關(guān)總署 國家體育總局令第9號)的有關(guān)規(guī)定執(zhí)行。
該目錄由兩大部分組成,第一部分為興奮劑品種,第二部分為對運(yùn)動員進(jìn)行興奮劑檢查的有關(guān)規(guī)定。興奮劑品種主要包括七類:蛋白同化制劑品種;肽類激素品種;麻醉藥品品種;刺激劑(含精神藥品)品種;藥品類易制毒化學(xué)品品種;醫(yī)療用毒性藥品品種以及其他品種。
掃描圖中二維碼
查看詳細(xì)信息

關(guān)于金振顆粒、婦科白鳳膠囊轉(zhuǎn)換為非處方的公告(2021年第3號)
根據(jù)《處方藥與非處方藥分類管理辦法(試行)》(原國家藥品監(jiān)督管理局令第10號)的規(guī)定,經(jīng)國家藥品監(jiān)督管理局組織論證和審定,金振顆粒、婦科白鳳膠囊由處方藥轉(zhuǎn)化為非處方藥。非處方藥說明書范本規(guī)定內(nèi)容之外的說明書其他內(nèi)容按原批準(zhǔn)證明文件執(zhí)行。藥品標(biāo)簽涉及相關(guān)內(nèi)容的,應(yīng)當(dāng)一并修訂。自補(bǔ)充申請備案之日起生產(chǎn)的藥品,不得繼續(xù)使用原藥品說明書。

掃描圖中二維碼
查看詳細(xì)信息

關(guān)于發(fā)布婦科調(diào)經(jīng)片中金胺O檢查項補(bǔ)充檢驗方法等3項補(bǔ)充檢驗方法的公告(2020年 第151號)
根據(jù)醫(yī)療器械風(fēng)險評價結(jié)果,為進(jìn)一步提升用械安全,消除風(fēng)險隱患,國家藥監(jiān)局決定進(jìn)一步規(guī)范醫(yī)用超聲耦合劑產(chǎn)品說明書及標(biāo)簽。
掃描圖中二維碼
查看詳細(xì)信息

CFDI
本周共計112+23+7個品種獲批取得藥品批準(zhǔn)證明文件,其中一致性評價品種46個。
藥品注冊申請藥學(xué)研制和生產(chǎn)現(xiàn)場檢查任務(wù)信息公告 (2020年第23號)
掃描圖中二維碼
查看詳細(xì)信息

藥品注冊申請藥學(xué)研制和生產(chǎn)現(xiàn)場核查任務(wù)信息公告 (2020年第24號)
掃描圖中二維碼
查看詳細(xì)信息

本周安康欣膠囊、銀屑膠囊、注射用萘普生鈉、滋陰益胃膠囊、萘普生鈉顆粒、萘普生鈉片、萘普生鈉、萘普生、補(bǔ)血生乳顆粒等國家藥品標(biāo)準(zhǔn)公示如下:
掃描圖中二維碼
查看詳細(xì)信息

-END-
關(guān)于我們:
藥政部是隸屬于公司副總裁直接領(lǐng)導(dǎo)下的部門,以國家藥品政策為導(dǎo)向,以為客戶提供集藥物研發(fā)、注冊申報、現(xiàn)場核查等一體化專業(yè)技術(shù)服務(wù)為宗旨,以高效、成功申報項目最終目標(biāo)。
藥政部擁有一支技術(shù)與注冊經(jīng)驗豐富的團(tuán)隊,作為一家提供專業(yè)服務(wù)的公司,在原料藥登記、仿制藥一致性評價、仿制藥注冊、新藥注冊以及進(jìn)口藥品注冊等方面均具有專業(yè)且豐富的經(jīng)驗,已助力成功申報多項藥品注冊申請,在業(yè)內(nèi)具有良好的口碑。
部門堅持 “忠誠、思考、建設(shè)、承擔(dān)、分享”的公司理念,不斷加強(qiáng)人才隊伍建設(shè)、提升專業(yè)能力、豐富注冊經(jīng)驗、拓展業(yè)務(wù)范圍,致力于為客戶提供高效率、高質(zhì)量、合規(guī)的技術(shù)服務(wù),為保護(hù)和促進(jìn)公眾健康而不懈努力。


轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務(wù)熱線:010-61006450
Hotline服務(wù)熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
