政策法規||本周重磅政策法規概覽(21.01.18-01.22)
CDE
關于發布《治療絕經后骨質疏松癥創新藥臨床試驗技術指導原則》的通告(2021年第2號)
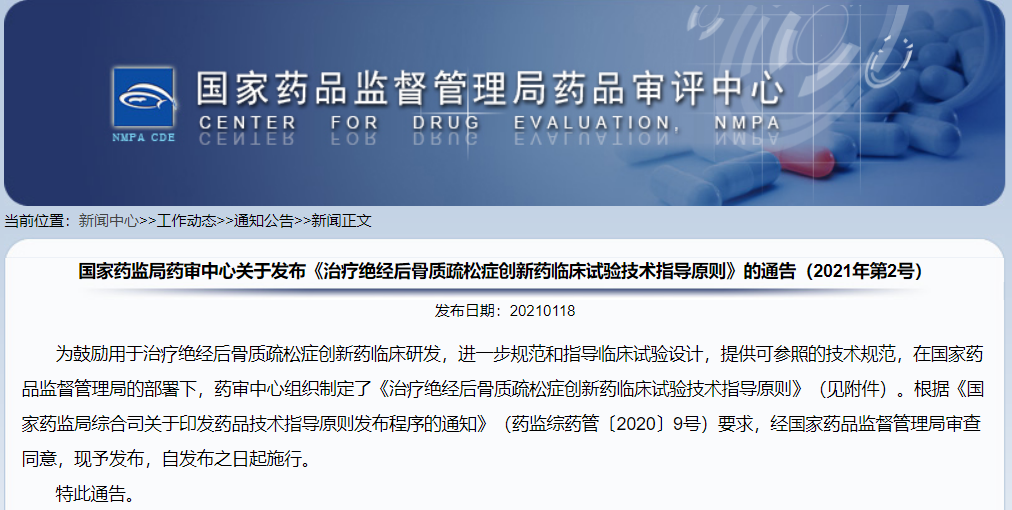
掃描識別下方二維碼
查看具體信息

NMPA
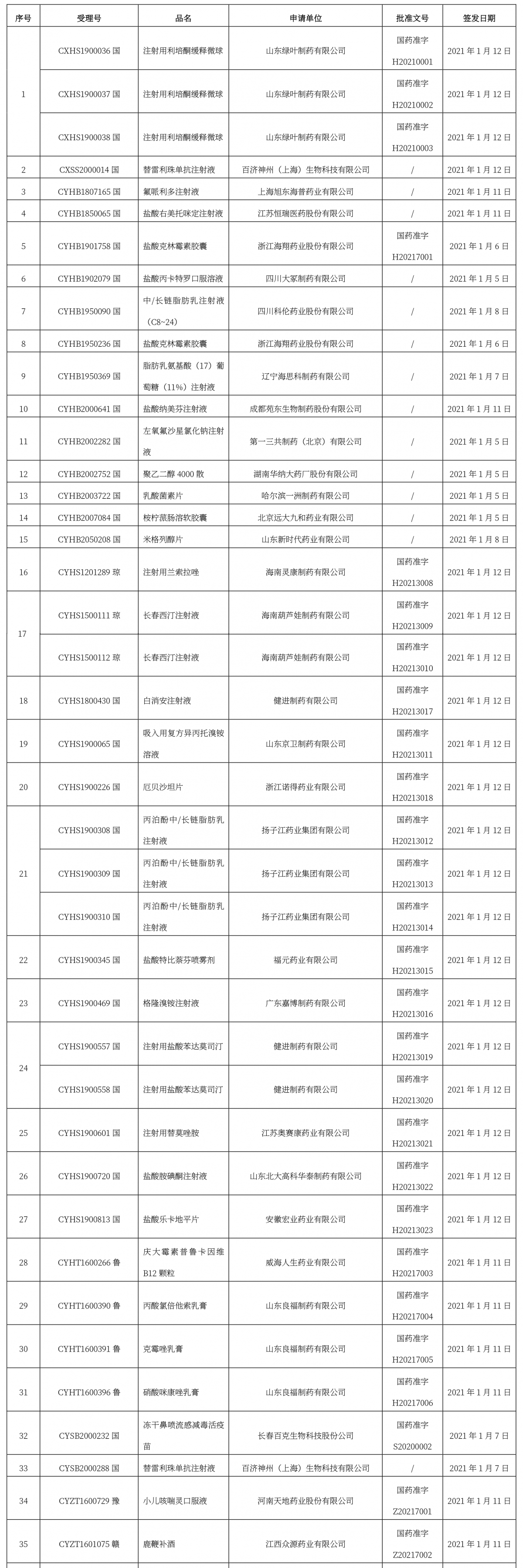
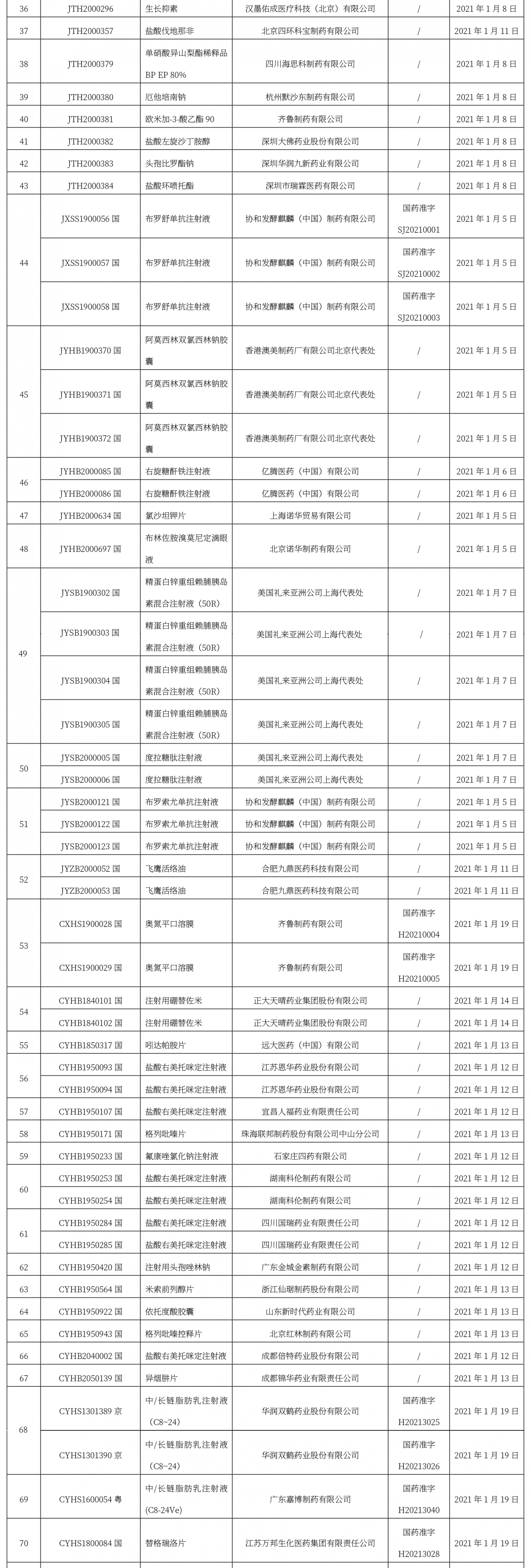
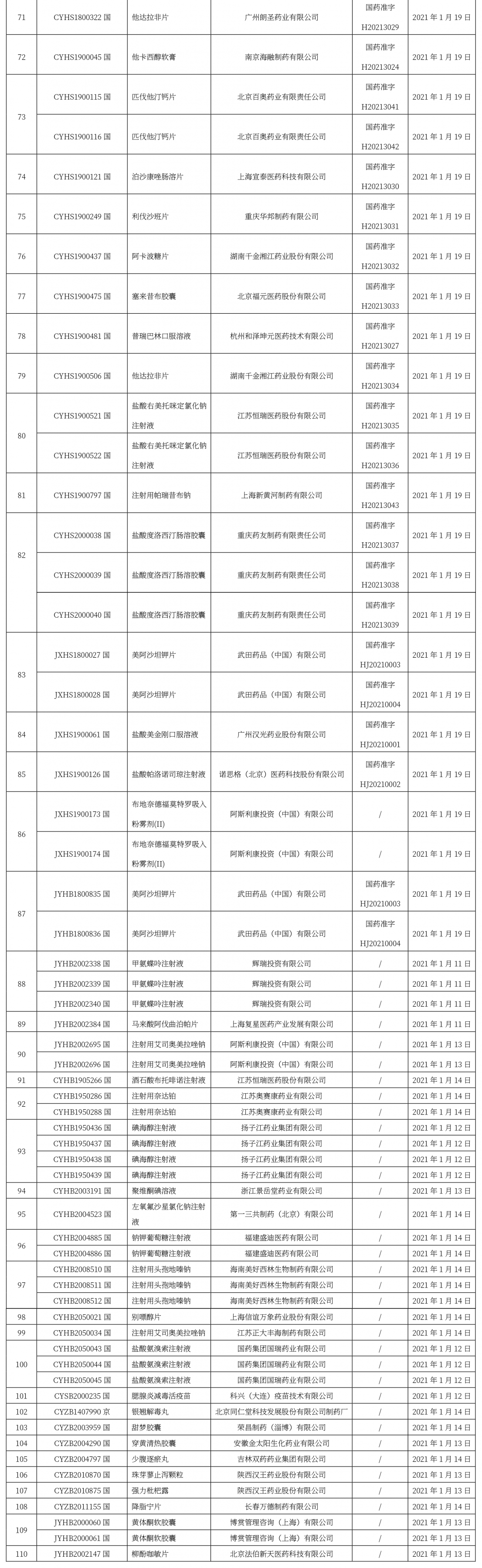
本周共計110 +62個品種獲批取得藥品批準證明文件(特殊藥品批文62個),其中一致性評價品種23個,注射劑品種45個。
關于對第二批重點實驗室名單進行公示的通知
掃描識別下方二維碼
查看具體信息

2021年1月20日中藥品種保護受理公示

掃描識別下方二維碼
查看具體信息

關于北芪片轉換為非處方藥的公告(2021年第14號)
掃描識別下方二維碼
查看具體信息

關于發布肺炎支原體IgM/IgG抗體檢測試劑等3項注冊技術審查指導原則的通告 (2021年第4號)

掃描識別下方二維碼
查看具體信息

關于布地奈德鼻噴霧劑處方藥轉換為非處方藥的公告(2021年第13號)

掃描識別下方二維碼
查看具體信息

關于修訂速效救心丸說明書的公告(2021年 第12號)
掃描識別下方二維碼
查看具體信息

關于批準注冊155個醫療器械產品的公告(2020年12月)(2021年 第10號)
掃描識別下方二維碼
查看具體信息

關于修訂帕米膦酸二鈉注射劑說明書的公告(2021年 第9號)
掃描識別下方二維碼
查看具體信息

關于修訂濕毒清制劑說明書的公告(2021年 第5號)
掃描識別下方二維碼
查看具體信息

關于修訂血府逐瘀制劑說明書的公告(2021年 第4號)
掃描識別下方二維碼
查看具體信息

關于發布免于進行臨床試驗醫療器械目錄(第二批修訂)的通告(2021年 第3號)

掃描識別下方二維碼
查看具體信息

關于發布影像型超聲診斷設備同品種臨床評價技術審查指導原則等2項注冊技術審查指導原則的通告(2021年 第2號)

掃描識別下方二維碼
查看具體信息

-END-
關于我們:
藥政部是隸屬于公司副總裁直接領導下的部門,以國家藥品政策為導向,以為客戶提供集藥物研發、注冊申報、現場核查等一體化專業技術服務為宗旨,以高效、成功申報項目最終目標。
藥政部擁有一支技術與注冊經驗豐富的團隊,作為一家提供專業服務的公司,在原料藥登記、仿制藥一致性評價、仿制藥注冊、新藥注冊以及進口藥品注冊等方面均具有專業且豐富的經驗,已助力成功申報多項藥品注冊申請,在業內具有良好的口碑。
部門堅持 “忠誠、思考、建設、承擔、分享”的公司理念,不斷加強人才隊伍建設、提升專業能力、豐富注冊經驗、拓展業務范圍,致力于為客戶提供高效率、高質量、合規的技術服務,為保護和促進公眾健康而不懈努力。


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
