榜上有名||北京新領先CXO 新征程
一、導讀
北京新領先醫藥科技發展有限公司作為全國工商聯醫藥業商會“研發及服務分會”會長單位,值此分會“藥全聯”公眾號上線之際,恰逢“第二屆中國生物醫藥創新合作大會”召開,謹以此篇文章吹響CXO集結號。
2020年6月19日“第二屆中國生物醫藥創新合作大會”上,由北京新領先臨床醫學部總監朱浩彬博士就 “縱向一體化CXO公司在中國藥物創新中的成果轉化作用”做主題發言,宣布新領先正式步入CXO時代!
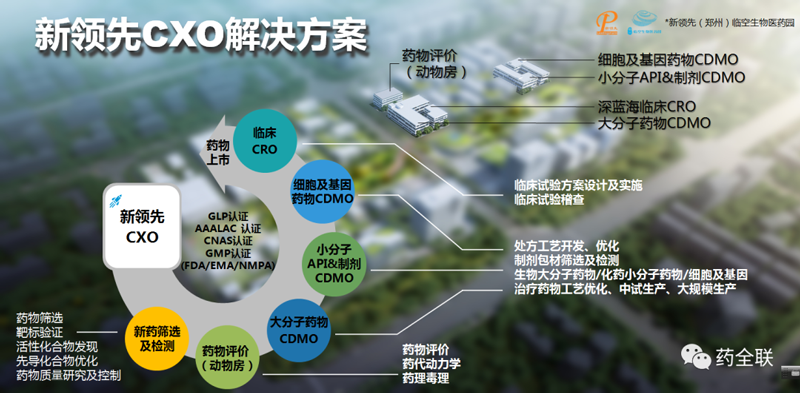
新領先醫藥作為全產業鏈的CRO公司,創建十六年,在臨床前研究、臨床CRO研究、IVIVR體內外橋接和進出口注冊等領域,一直處于領先地位,連續三年被評為“中國醫藥研發公司10強(前三強)”,并于2015年實現主板上市。
步入2020年,新領先厚積薄發,依托既有的技術和管理團隊,整合鄭州臨空生物醫藥產業園平臺,全面入資,建設并運營六大技術平臺,全面覆蓋醫藥研究、委托加工及質量控制等醫藥全流程,為全球客戶提供真正意義上的一站式服務。
二、平臺介紹
(1)新藥篩選及檢測平臺
新藥篩選及檢測平臺是醫藥研發和創新的基礎。建立配備HPLC、UPLC、GC/GC-MS、LC-MS、ICP-MS、TGA、溶出儀、核磁等先進大型精密儀器設施的高標準研發實驗室。為新藥實驗開發提供有力保障。
服務內容:高通量藥物篩選、活性化合物發現、靶標驗證、先導化合物優化、臨床前候選藥物選擇等技術研發服務,并以數據庫支持整個體系運轉,大幅度地縮短新藥發現的時間,增加高特異性、高活性藥物的發現率,促使新藥流程快速進入候選物的確定和新藥臨床研究,有效幫助客戶控制新藥開發成本。
(2)藥物評價平臺(動物房)
藥物評價平臺(動物房)按照國際化標準設計建造,平臺共5層,總建筑面積4920.75m2,能夠滿足AAALAC、中國GLP、CNAS要求。
服務內容:藥物發現、化學合成、生物分析、PKPD模型擬合、大分子藥、臨床申報、毒性毒理、藥代動力學、藥效學以及細胞/基因治療藥物體內外藥效評價、DMPK等。
(3)大分子中試及大規模生產服務平臺
大分子中試及大規模生產服務平臺共4層,總建筑面積11453 m2,符合美國FDA、歐盟EMA和中國NMPA GMP標準,旨在為生物大分子藥物提供研發生產一體化CDMO服務。
服務內容:穩定細胞系篩選、中試發酵工藝、大規模培養工藝及大分子純化工藝開發服務,抗體藥物、重組蛋白藥物、蛋白疫苗中試和大規模生產服務,生物大分子藥物制劑的生產技術服務,支撐產品在中、美、歐等地同時進行臨床試驗并快速上市,實現客戶的研究成果全球同步轉化。
(4)小分子CMC制劑研究生產平臺
小分子CMC制劑研究生產平臺總建筑面積6651.54m2,符合美國FDA、中國NMPA GMP標準,具有面向國際市場服務能力的小分子制劑研究、臨床樣品生產及商業化生產能力。
服務內容:難溶性藥物解決方案、規口服和注射給藥劑型的中試試驗(片劑、膠囊、顆粒劑、小容量注射液、注射用凍干粉等)、臨床樣品生產及商業化生產服務,支撐創新藥企、MAH持有人及仿制藥研發公司進行創新藥研發、仿制藥一致性評價和研發申報。
(5)細胞技術服務平臺
細胞技術服務平臺總建筑面積6651.54m2,符合美國FDA、歐盟EMA和中國NMPA GMP標準,可滿足細胞與基因治療藥物的小試、中試及商業化生產需要。
服務內容:細胞與基因治療藥物(質粒、病毒、細胞藥物形式)全流程CDMO服務——小試、中試、臨床前研究、IND注冊申報、臨床試驗及商業化藥品生產,干細胞免疫細胞存儲,專項質量檢測指標的開發和檢測,并可為醫療機構、研發機構等提供質粒、慢病毒載體的現貨供應及細胞制劑的制備服務。
(6)臨床CRO服務平臺
臨床CRO平臺具有ICH-GCP臨床研究質量管理體系和標準操作規程(SOP),通過ISO9001質量標準認證。全面覆蓋大小分子藥物、滿足不同需求研發型企業的臨床研究。
服務內容:創新藥和仿制藥的Ⅰ~Ⅳ期臨床試驗、仿制藥生物等效性(BE)試驗及藥代動力學(PK/PD)臨床研究、體內外相關性研究(IVIVR)、醫療器械臨床研究及第三方稽查等,為國內外客戶打通新藥上市前關鍵瓶頸。
三、結語
新領先醫藥將于2020年9月25日~27日,與河南省有關部門及生物園區共同舉辦“第二屆鄭州國際生物藥高峰論壇”,屆時,我們將逐一展示我們的CXO版塊,歡迎各界同仁光臨指導!
轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
