新領先醫藥,讓您的注射劑一致性評價走在集采前列
一、市場格局
全國注射劑市場中,化藥注射劑占整體市場的72%左右。米內網數據顯示,2019年中國化藥注射劑市場規模突破6300億!
到目前為止已進行的3次國家帶量采購,每次都會涉及注射劑品種。集中采購是仿制藥大勢所趨,而通過一致性評價則是進入集采的入場券。注射劑不同于口服制劑,其銷售終端基本都在醫院,一旦因不過評而暫停掛網或無緣參與集采,那就意味著基本失去了市場。
二、形勢嚴峻
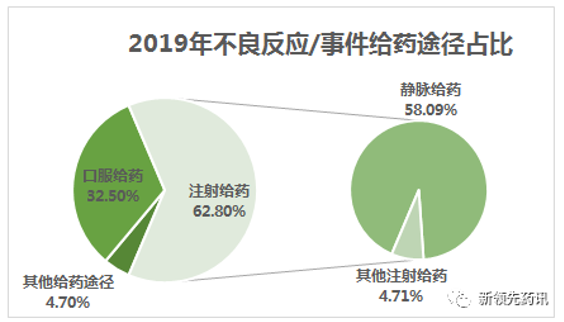
由于歷史因素,國產注射劑的安全性和有效性與原研制劑之間仍存在差異。根據《國家藥品不良反應監測年度報告(2019)》統計顯示,在2019年不良反應/事件報告中,注射劑占62.8%(其中靜脈給藥58.09%,其他注射給藥4.71%),口服給藥占32.5%,其他給藥途徑占4.7%。
一致性評價工作的開展使得國產仿制藥質量和療效與原研制劑相同,是有利民生的大事,對藥品的安全性和有效性負責更是上市持有人要承擔的責任。
時限要求:化學藥品新注冊分類實施前批準上市的含基本藥物品種在內的仿制藥,自首家品種通過一致性評價后,其他藥品生產企業的相同品種原則上應在3年內完成一致性評價。逾期未完成的,企業經評估認為屬于臨床必需、市場短缺品種的,可向所在地省級藥品監管部門提出延期評價申請,經省級藥品監管部門會同衛生行政部門組織研究認定后,可予適當延期。逾期再未完成的,不予再注冊。
三、機遇暗藏
據了解,國內很多注射劑批文屬于三改品種,與參比制劑的安全性和有效性存在一定差距。擁有這些品種的企業,若想要繼續生存,有必要結合自身的生產能力,按照新的技術要求開展與原研制劑一致的仿制藥立項研究,在新的法規形式下仍有與開展一致性評價的企業公平競爭的機會。
Insight數據顯示,截止2020年5月30日,已通過(含視同通過)一致性評價的品種共計33個,涉及受理號60個;已提交補充申請的品種共計153個,涉及受理號884個。已獲批的文號僅占全部提交申請的6.36%!注射劑一致性評價正式稿落地之前,相關法規政策均為征求意見稿,法規政策的不明朗導致已經申報的大部分注射劑項目未開展實質性審評,導致審評積壓,并且提交審評的項目多存在發補情況。注射劑一致性評價正式稿落地,對相關技術指導原則加以明確,再結合已有申報項目的豐富經驗,使得再開展的注射劑項目可在很大程度上縮短研發和審評時間,這也就給了后續開展注射劑研究工作的廠家以新的機遇。
那么,應該在何時開展注射劑一致性評價工作,才能躋身未來市場呢?我們來算一筆時間的賬!
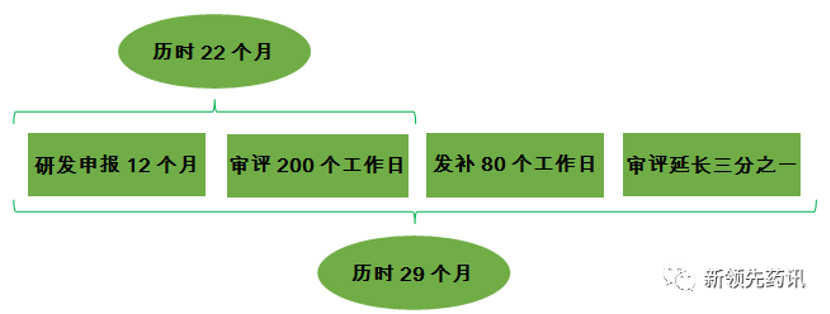
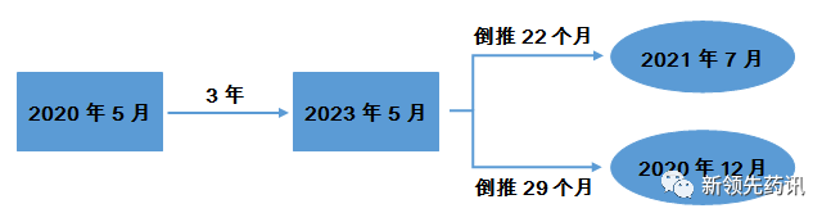
已有批文過評的品種:注射劑一致性評價從研發到獲批,共計需要22個月左右(不發補)。正式稿于2020年5月14日發布,3年時限到2023年5月13日。從2023年5月倒推22個月,得到答案:2021年7月!如果發補,需要增加發補時間加延長審評周期共7個月左右,得到答案:2020年12月!保險起見,相關未開展的廠家在2020年12月之前開展相關研究工作,才能有望躋身未來市場!
已申報未獲批品種:此類品種多存在發補現象,從審評開始到獲批歷時17個月左右。假定從2020年6月開始進入審評,大概率在2021年11月左右獲批。未開展的廠家若從2020年6月開展研究工作,按照現行法規要求進行研發,歷時22個月左右時間獲批,也僅僅比已經做完研究的廠家晚5個月左右,有望躋身市場前列!
北京新領先:
北京新領先醫藥將團隊中液體制劑專業人才進行整合,成立專門針對注射劑一致性評價的液體制劑事業部,專注于凍干粉針、無菌分裝、水針劑、大輸液等品種的研究。
1.全過程風險控制,為您提供一站式服務
我公司具備從專業立項評估至獲得批件的全流程鏈的專業職能部門,為注射劑一致性評價項目的申報獲批保駕護航:
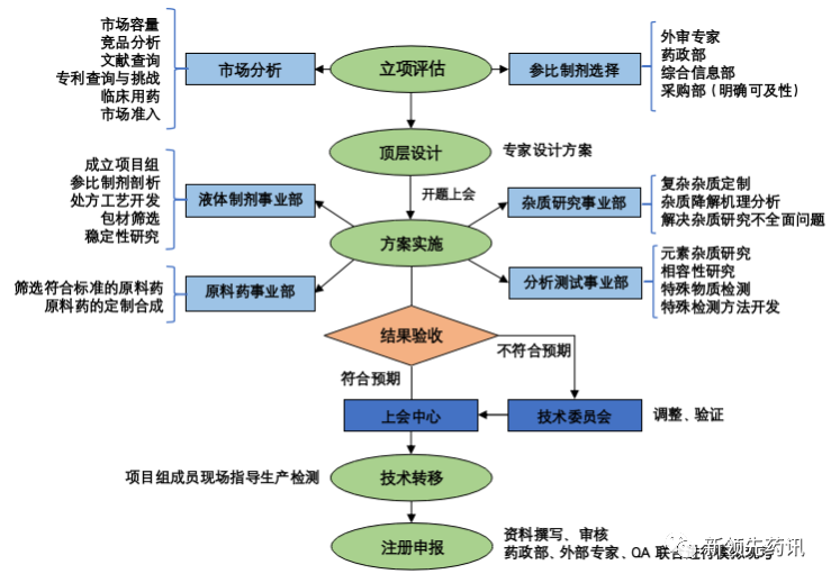
2.技術重難點把控,為您打破限速步驟
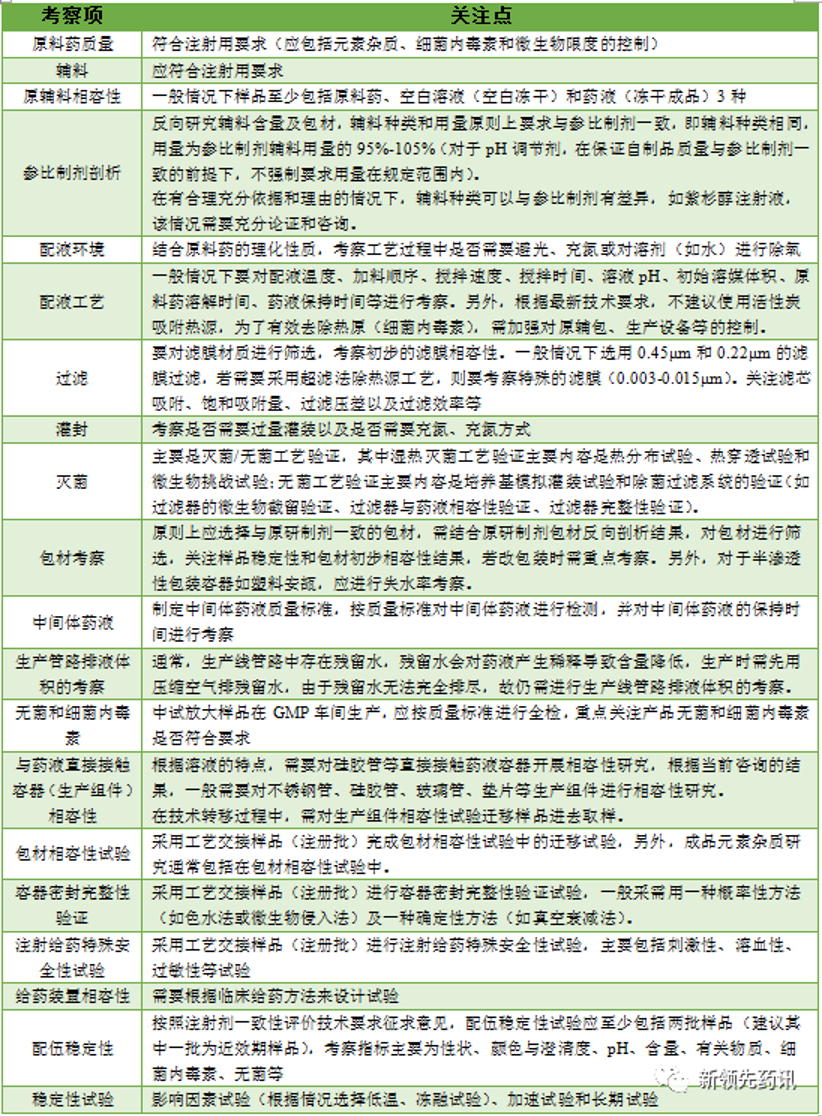
對于普通注射劑的仿制,不同于口服固體制劑,無需進行體外溶出擬合,但對于質量要求更為嚴格。需以輔料組成(Q1)相同,用量(Q2)相同(仿制藥輔料用量為參比制劑相應輔料用量的95%~105%)為前提,對原輔包的質量、滅菌工藝、配伍穩定性、安全性及相容性等進行嚴格的考察。
液體制劑事業部專注于注射劑的研發,對于整個研發過程中的重難點有深入研究,主要包括以下幾方面但不局限于以下:
3.100%優勢,讓項目安全落地
北京新領先通過ISO9001質量認證,完善的質量管理體系,對人機料法環各個環節進行嚴格的質量控制,最大限度確保項目的合規性。通過每一位研發人員的不懈努力,液體制劑工藝交接一次性成功率達到100%!研究和生產現場核查一次性通過率100%!真正做到“以客戶為本”,讓每個項目安全落地!
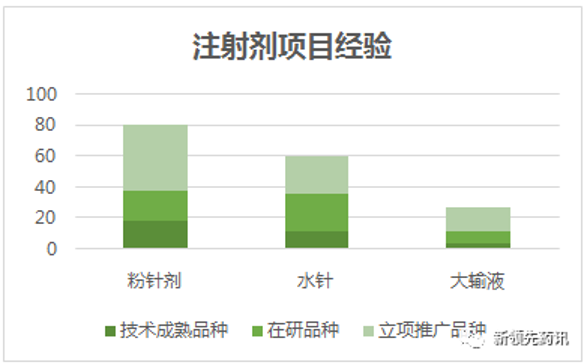
4.豐富的項目經驗,快速實現產業化
經過十余年的積淀,新領先醫藥目前已成功轉化注射劑品種近40項,如:注射用阿奇霉素、注射用頭孢曲松鈉、氨甲環酸注射液等;在研品種50余項,立項推廣品種80余項,豐富的注射劑項目經驗為后續項目研發提供了大量的經驗支持,能夠幫助企業快速實現產業化,帶您走入集采行列!
作為一家負責任的cro公司,我們與藥企之前呈現深度戰略綁定,最大限度參與藥企一致性評價的戰略規劃,最大限度降低藥企溝通成本、時間成本及評審風險,滿足并服務于藥企的戰略布局。新領先愿做您一致性評價道路上的戰略助推器,而不是一個戰略暗釘!新領先已經準備好,用我的戰略思維、人才技術厚度、管理延伸度以及行業話語度,全力護航您的一致性評價及企業戰略達成!
關于我們
液體制劑事業部現有研發人員80余人,近80%為碩士或博士學歷。由具有10年以上國內外項目管理、藥品開發及生產轉化經驗人員作為主要研究及管理者,形成從具有集產品立項、處方工藝開發、質量全面研究、工藝產業化、穩定性研究及注冊申報于一體的藥品研發全產業鏈架構。
事業部配備液體制劑開發所必備的成熟國際知名品牌的生產和檢測設備。分析檢測儀器包括卡爾費休水分測定儀、不溶性微粒檢測儀、澄明度檢測儀、自動表/界面張力儀、頂空氣體分析儀、數顯粘度計、馬爾文激光粒度儀、滲透壓測定儀、呼吸模擬器、新一代藥用多級撞擊器、醫用壓縮/超聲霧化器、溶解氧測定儀以及HPLC/UPLC/LC-MS/ICP-MS/GC/GC-MS等色譜、質譜或聯用等儀器。工藝開發及放大設備主要包括不銹鋼配制罐(具有加熱和冷卻功能)、囊式過濾器、安瓿熔封機、東富龍0.25㎡凍干機以及濕熱全自動高壓滅菌儀柜(可打印曲線及F0值)、密封性測試儀、多功能瓶蓋鎖口機、低溫超高壓均質機、真空手套箱等,可滿足實驗室研究及中試規模放大驗證使用,實現從實驗室研究至放大生產的零風險過渡。
轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
